vad är ett reducerande socker, och varför är det viktigt? Här är en snabb sammanfattning. Fullständiga detaljer i inlägget nedan.,
Innehållsförteckning
- innan vi talar om att minska sockerarter, Kemi ”Peeing på pinnen”
- Benedict’ s, Fehlings och Tollens ’ tester: tre visuella ”tester” för närvaron av aldehyder
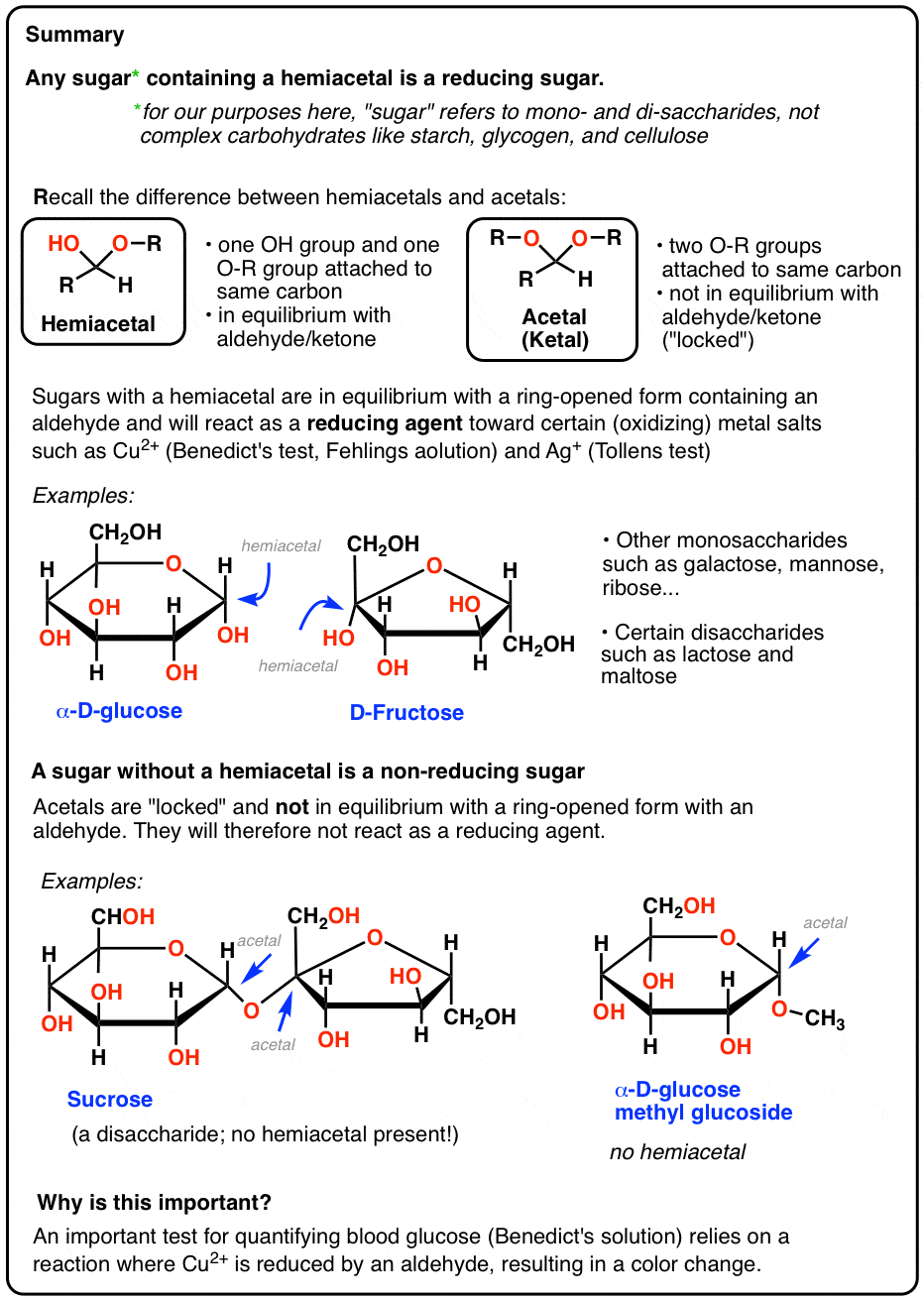
- reducerande sockerarter: sockerarter med en hemiacetal funktionell grupp ger positiva tester eftersom de är i jämvikt med en öppen-chain aldehyd
- så vad är inte en reducerande socker?
- sackarider som saknar Hemiacetal minskar inte sockerarter
- komplexa polysackarider med en enda Hemiacetal enhet (t. ex., Socker
- testa dig själv på reducerande sockerarter
- Kemi Benedict, Fehlings och Tollens tester
- anmärkningar
- (avancerade) referenser och ytterligare läsning
1. Innan vi pratar om att minska sockerarter: Kemin att ”kissa på pinnen”
Q. kan du tänka på en situation där det kan vara användbart att kunna mäta koncentrationen av glukos i en lösning (särskilt i blod eller urin) ?
A. Diabetes., När du har ett sätt att snabbt och enkelt mäta koncentrationen av socker kan du bestämma hur mycket insulin som behövs för att motverka det.
nästa fråga. Vad skulle vara ett enkelt, visuellt sätt att upptäcka närvaron av glukos? Speciellt något som inte kräver att du är en expert kemist?
helst Vill du ha en kemisk reaktion som resulterar i en färgförändring.
Tänk på graviditetstest: du kissar bara på en pinne och vet inom några minuter om du är gravid. Du behöver inte veta någon kemi. Det är hjärnlöst.,
ett test för blodsocker som är lämpligt för diabetiker bör ha en liknande användarvänlighet.
detta ger oss (via aldehyder) till ämnet reducerande sockerarter, eftersom de ligger till grund för ett historiskt viktigt färgbaserat test för blodglukos.,
tre visuella ”test” för närvaron av aldehyder: Benedicts, Fehlings och Tollens Test
innan vi kommer till sockerarter, låt oss prata om oxidationen av aldehyder.
Vi har tidigare sett att aldehyder är en funktionell grupp som kan oxideras relativt lätt till karboxylsyror. Till exempel resulterar oxidation av alkoholer med en ”stark” oxidant som kromsyra (H2CrO4) i en aldehyd som snabbt oxideras vidare till en karboxylsyra.
under denna process oxideras aldehyden och oxidationsmedlet reduceras., Ett annat sätt att inrama detta är att säga att aldehyden är reduktionsmedlet i denna process.
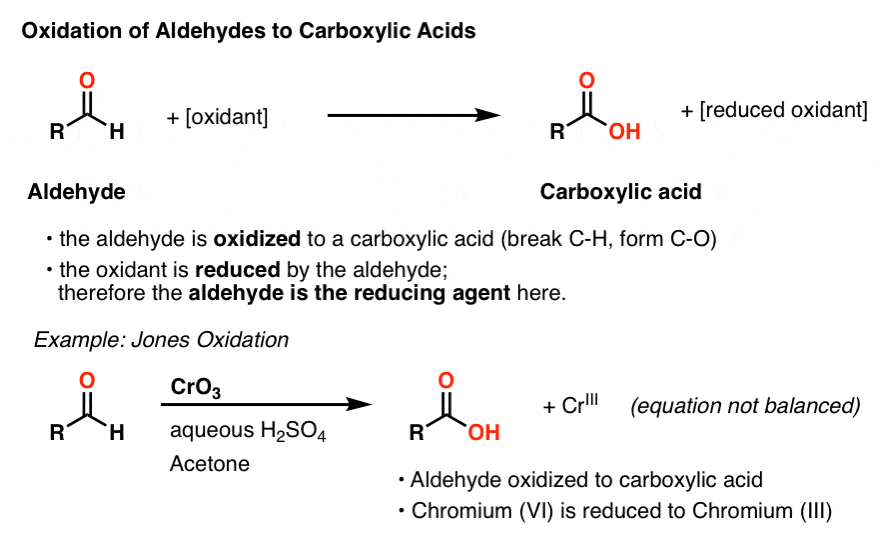
listan över reagenser som kan användas för att oxidera aldehyder till karboxylsyror är loooong. Av dessa utmärker sig några metoder för att ge en särskilt tydlig visuell indikation på att reaktionen har gått vidare till slutförandet.
tre ”visuella” test för aldehyder som du kan stöta på i ett inledande organiskt kemilabb är följande:
- Fehlings lösning, där en aldehyd ändrar färgen på en blå cu(II) lösning till röd cu(i) .,
- Benedicts lösning en något modifierad version av Fehlings lösning
- Tollens test, där aldehydoxidation resulterar i en vacker ”spegel” av silvermetall för att fälla ut på reaktionskärlet.
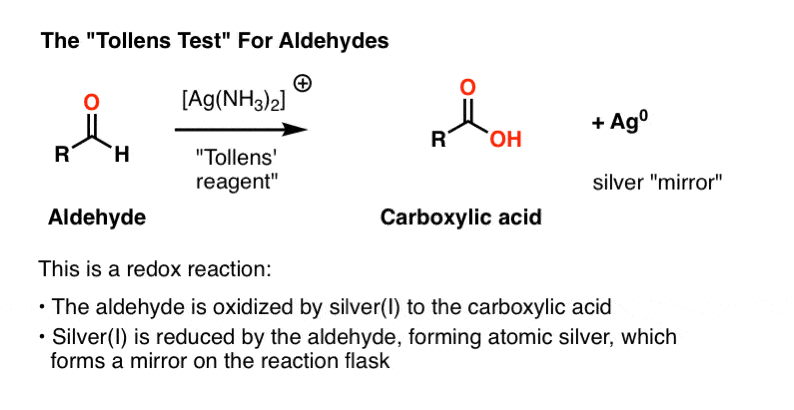

viktigt är att ketoner inte reagerar under något av dessa förhållanden. Ovanstående tester var också ett användbart sätt att skilja aldehyder från ketoner i de mörka dagarna innan IR och NMR-spektroskopi gjorde denna rutin.
Så vad har detta att göra med sockerarter?, Låt oss gå tillbaka till skrikande läge:
reducerande sockerarter: sockerarter med en hemiacetal funktionell grupp ger positiva tester eftersom de är i jämvikt med en öppen kedja aldehyd
som vi har sett är glukos i jämvikt med en öppen kedja (eller ”linjär”) form som innehåller en aldehyd.
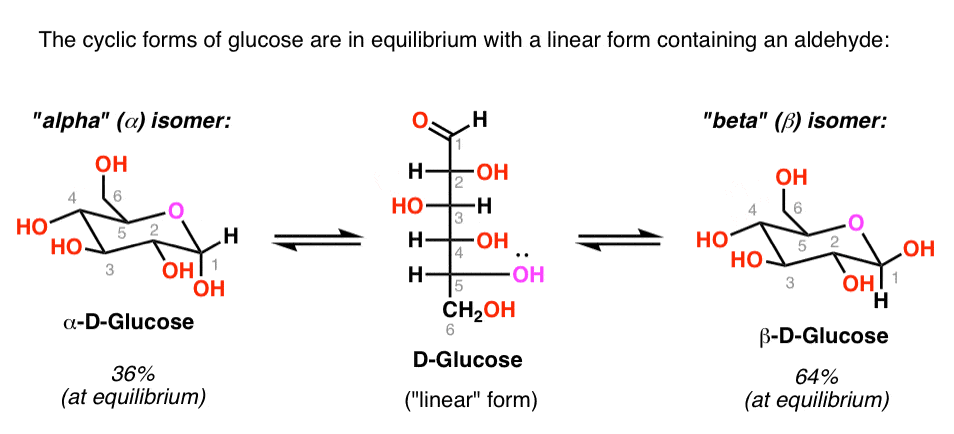
koncentrationen av aldehyd vid varje given tidpunkt är liten (<1%), men tillräckligt länge för att fångas med rätt reagens.,
detta innebär att glukos kommer att ge ett positivt test med Benedicts reagens, fehlingslösning eller Tollens-testet och aldehyden kommer att oxideras till en karboxylsyra.
Voila! En enkel färgförändring berättar om glukos är närvarande!

bildkälla
vad sägs om kvantifiering?
det är trevligt att ha ett snabbt visuellt test för glukos., Men vad händer om vi vill bestämma den exakta koncentrationen av glukos i en lösning av, säg, urin eller blod?
i detta fall används en något annorlunda formulering av Benedicts lösning som resulterar i en färglös fällning snarare än en röd färg. En lösning av provet som ska analyseras tillsätts, via buret, till en kolv som innehåller en känd mängd Benedicts-lösning tills den blå färgen på Cu(II) försvinner. Det okända provet kalibreras sedan med en 1% glukoslösning.
Benedicts-analysen var den metod som användes för att kvantifiera glukos i över 50 år., En forskare påminner om att alla invalda i den amerikanska armén under andra världskriget hade sin urin testad för socker med Benedicts lösning.
På senare tid har dock användningen av Benedicts lösning ersatts av enzymatiska metoder som glukosoxidas. Varför?
Benedict-testet är inte specifikt för glukos; det berättar bara om en aldehyd är närvarande. Så det kommer också att ge ett positivt test för andra reducerande sockerarter.,
kort sagt, något socker* (*mono – eller disackarid) med en hemiacetal kommer också att ge ett positivt test, eftersom dessa sockerarter är i jämvikt med en öppen kedja aldehyd. Så om blod/urin innehåller vanliga monosackarider som mannos, galaktos eller fruktos, kommer dessa att leverera ett positivt test. Med andra ord minskar dessa sockerarter också sockerarter. 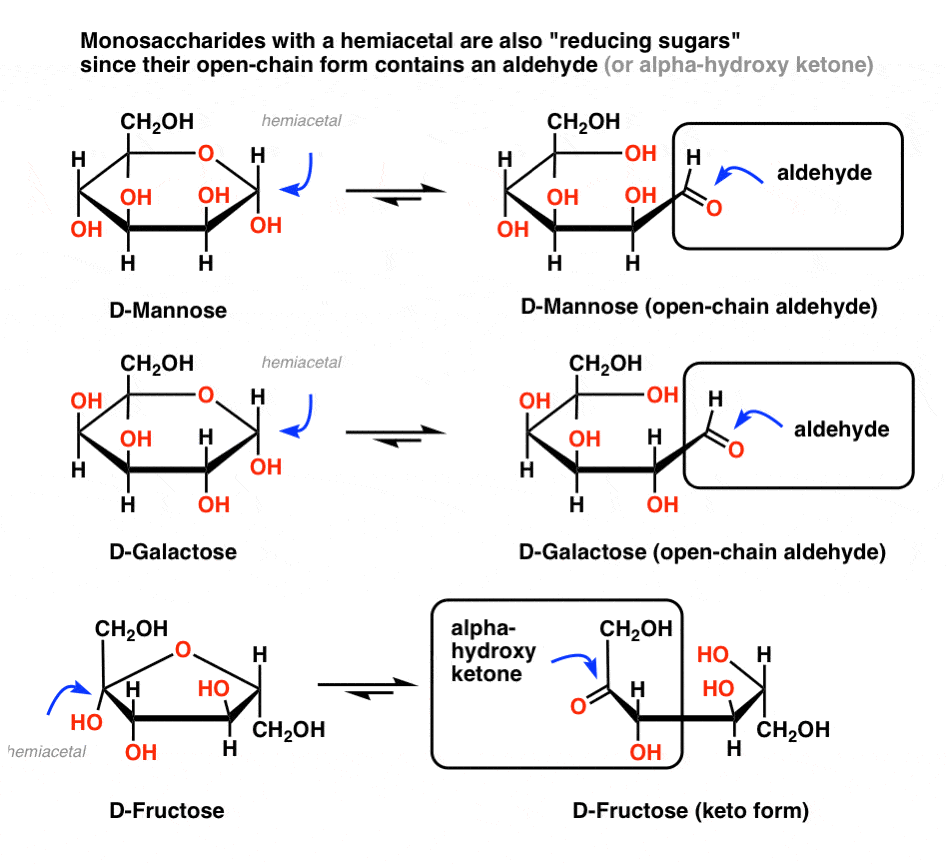
håll kvar en sekund. Et tu, fruktos?
ketoner är inte tänkt att oxidera under dessa förhållanden! Så varför ger fruktos ett positivt test?
bra fråga., Även om fruktos är ett ketosocker, och ketoner ger i allmänhet ett negativt test med Benedict, finns det ett undantag. Om kolet intill ketonkol (”alfa-kol”) innehåller en hydroxylgrupp, kommer ketonen att vara i jämvikt med en aldehyd genom tautomerisering (bara för rekordet kallas detta en ”enediol-ombildning”).
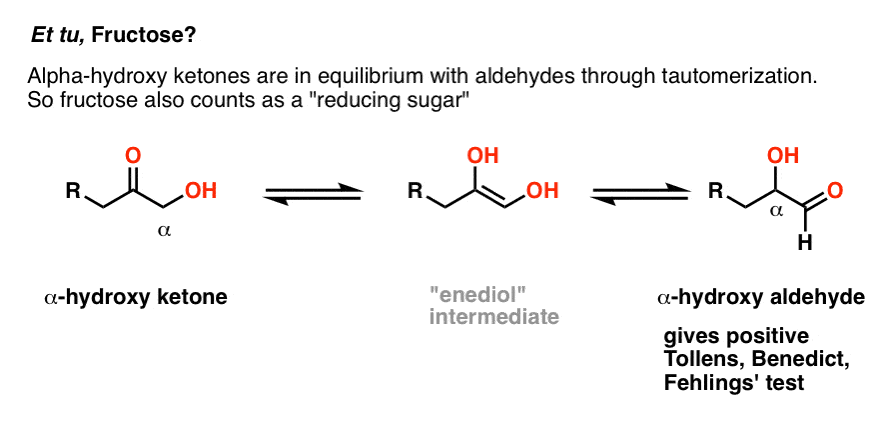
På samma sätt innehåller vissa disackarider som maltos och laktos en hemiacetal., De minskar också sockerarter som ger ett positivt Fehlings, Benedict eller Tollens test (bilden av laktos positivt test är längre ner).
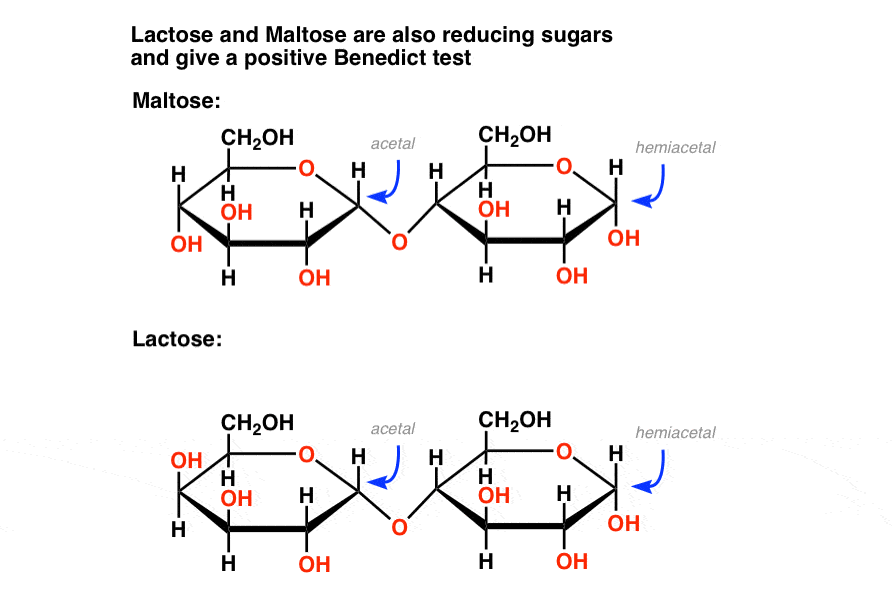
grunden är att Benedicts reagens kvantifierar reducerande sockerarter som inte bara innehåller glukos utan även mannos, laktos, maltos, fruktos och andra. Det betyder att testet inte är så specifikt som vi skulle vilja!
så vad är inte ett reducerande socker?
hittills verkar det som om varje socker Vi har stött på är ett reducerande socker. Så det är rättvist att fråga: när är ett socker inte ett reducerande socker?,
två huvudfall:
- mono och di-sackarider som saknar hemiacetal
- polysackarider där förhållandet mellan hemiacetaler och acetalbindningar är mycket lågt (t.ex. stärkelse)
sackarider som saknar Hemiacetal minskar inte sockerarter
vi såg på toppen av posten att hemiacetaler är i jämvikt med en aldehyd eller keton. Däremot låses acetaler (ketaler) på plats och kan endast omvandlas tillbaka till aldehyd eller keton med vattensyra. Det är därför de gör bra skyddsgrupper för aldehyder / ketoner.,
affischen barn för en icke-reducerande socker är sackaros, Alias bordssocker.
sackaros är en disackarid av glukos och fruktos. Se om du kan hitta en hemiacetal i sin struktur, nedan:
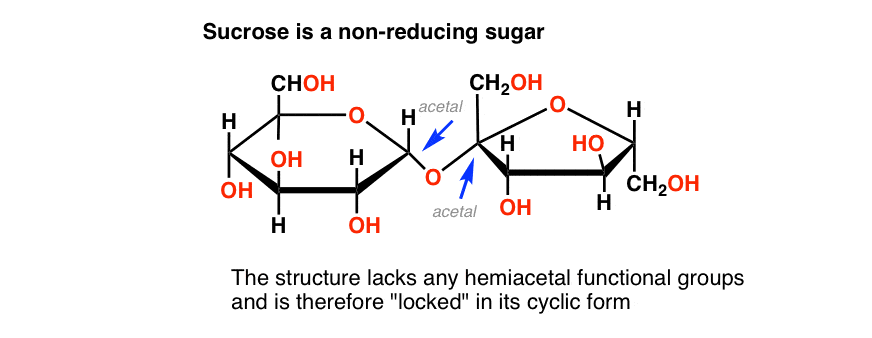
det finns ingen! Sackaros har bara acetalgrupper, och eftersom acetaler inte öppnar sig för aldehyder under de grundläggande förhållandena som finns i Benedict-testet är sackaros inte ett reducerande socker.
sackaros ger ett negativt test (blått) till Benedict-lösningen.,
ett annat exempel på ett icke-reducerande socker är de så kallade ”glukosiderna” av vanliga sockerarter, såsom glukosmetylglukosid, nedan. Detta erhålls genom uppvärmning av glukos i sur metanol.
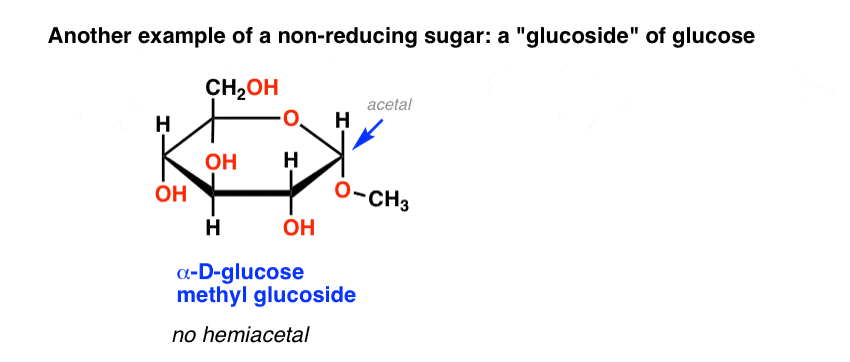
saknar en hemiacetal som kan öppna för en aldehyd, ger denna metylglukosid också en negativ Benedicts test.
komplexa polysackarider som endast har en enda Hemiacetal enhet räknas inte som reducerande sockerarter (t. ex. stärkelse)
sockerarter kan bilda långa kedjor med varandra i arrangemang som kallas polysackarider., Vanliga exempel på polysackarider är stärkelse, cellulosa och glykogen.
de allra flesta enskilda sockerenheter i dessa polysackarider är förenade med varandra via acetal (”glykosidbindningar”). Hemiacetaler är närvarande, men endast vid polymerens termini.
stärkelse, till exempel, har i allmänhet cirka 300-600 enskilda enheter glukos, men endast en enhet (terminusen) har en hemiacetal.
en hemiacetal ”nål” i en höstack av ”acetaler” räcker inte för att ge ett positivt test för att minska sockerarter. Därför anses dessa polysackarider inte vara reducerande sockerarter., Stärkelse ger till exempel ett negativt test (se nedan).
Här är ett exempel på Benedicts test med laktos, stärkelse, glukos, fruktos och sackaros (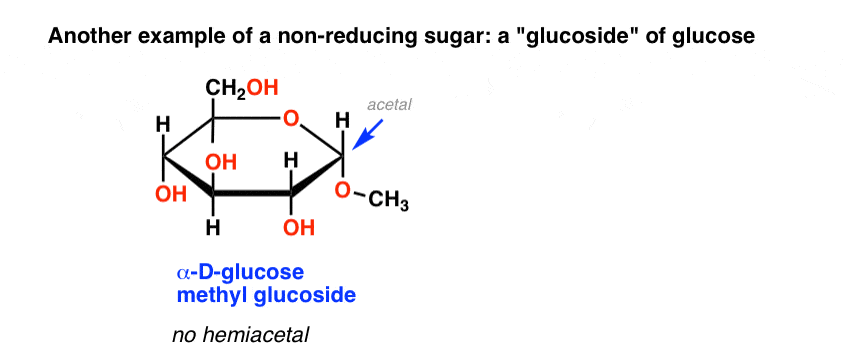
Observera att stärkelse och sackaros är blå och klassificerar dem som icke-reducerande sockerarter.
det räcker med vad som klassificerar ett ”reducerande socker” från ett ”icke-reducerande socker”.
här är det sista steget. Testa dig själv. Vad är en reducerande socker och vad är inte?
7. Testa dig själv på att minska sockerarter
vettigt? Quiz själv om följande sockerarter minskar sockerarter eller icke-reducerande sockerarter.,
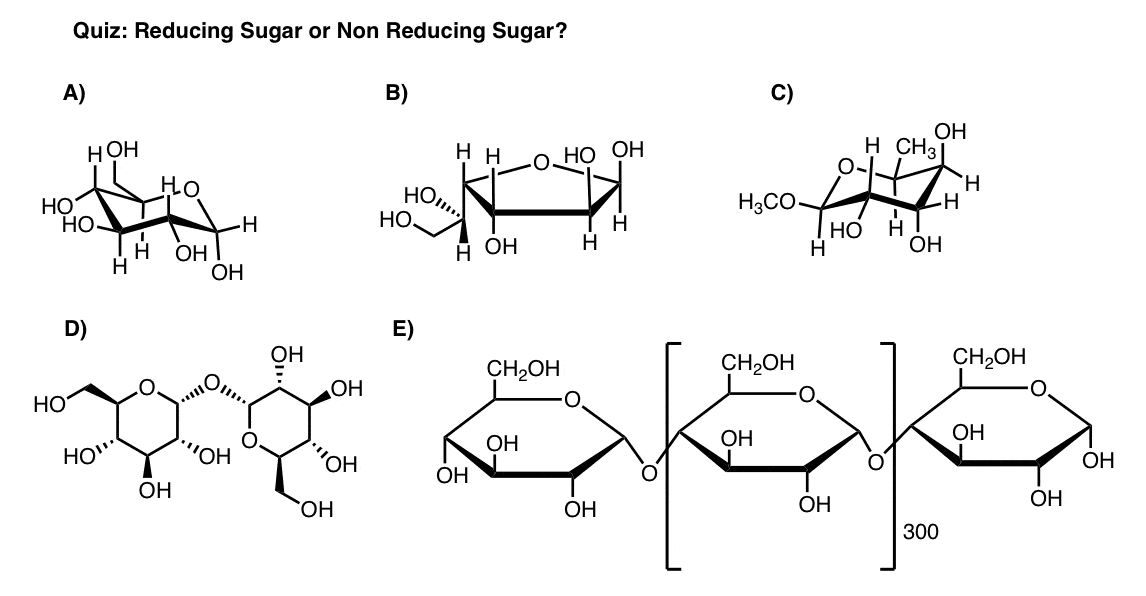
om du inte behöver veta något annat än ”vad är ett reducerande socker”, är du klar här.
men om du vill gå längre ner i kaninhålet, jag inbjuder dig att läsa vidare för att lära sig om…
Kemi Benedict, Fehlings och Tollens tester
Så vad händer egentligen i Benedict, Fehlings och Tollens tester? Låt oss diskutera detaljerna i kemin.
en sak med alla tre testerna är att det aktiva reagenset inte är särskilt stabilt och måste vara nyberedd.,
Fehlings lösning
För Fehlings lösning börjar man med klarblå koppar(II) sulfat, natriumhydroxid och kaliumnatriumtartrat (annars känt som Rochelle ’ s salt). Syftet med att använda tartratet är att det samordnar till koppar (II) och hjälper till att förhindra att det kraschar ur lösningen.
efter beredning tillsätts det ämne som ska analyseras och blandningen upphettas under en kort period.
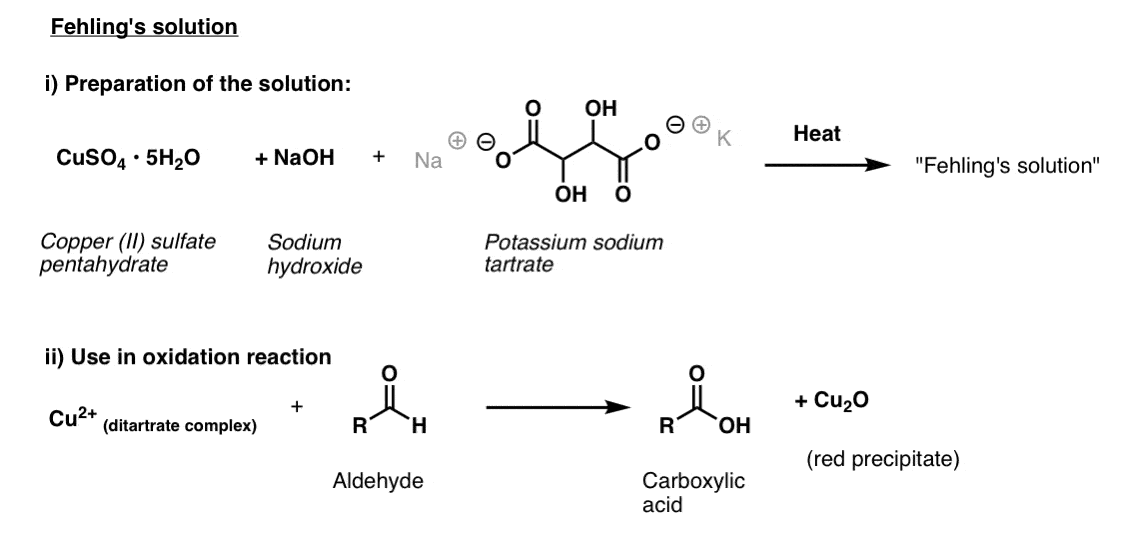
detta resulterar i en karboxylsyra och röd cu(I) som fälls ut som koppar(i) oxid.,
strukturen hos den aktiva arten i Fehlings lösning har bestämts; det är ett fyrkantigt kopparkomplex som är fäst vid två tartratligander.
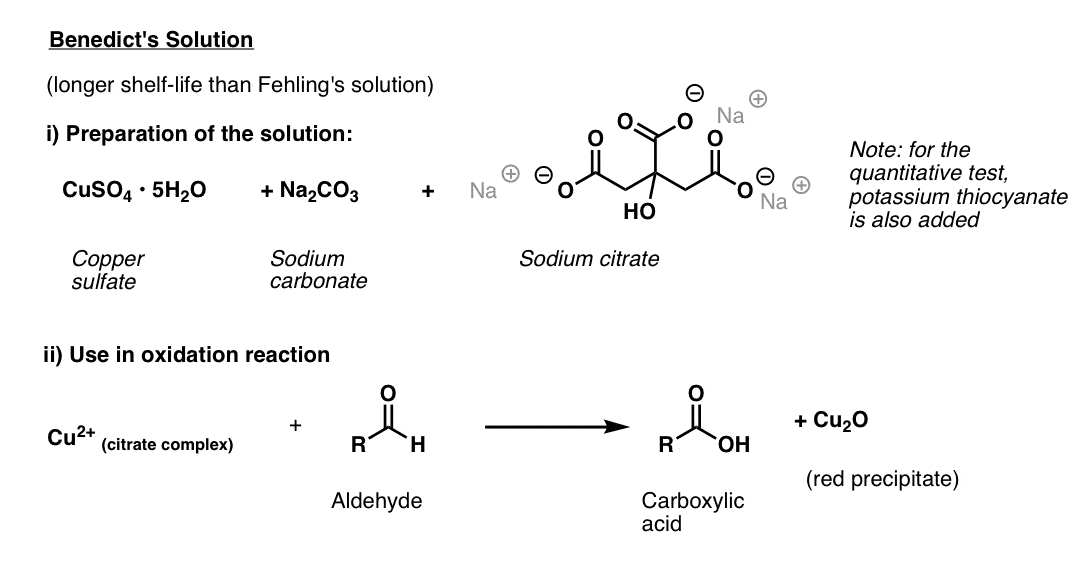
Benedicts lösning
Benedicts lösning är en liten variation av Fehlings lösning som använder citrat istället för tartrat, vilket ger bättre stabilitet för koppar(II).
liksom Fehlings lösning är det bäst gjort färskt. Ingredienserna är koppar (II) sulfat, natriumkarbonat (Obs: hydroxid behövs också! – se referens) och natriumcitrat., (Anm.: i det kvantitativa testet tillsätts kaliumtiocyanat, vilket resulterar i en färglös vit fällning).
testet utförs genom tillsats av ämnet som ska analyseras och uppvärmning kort.
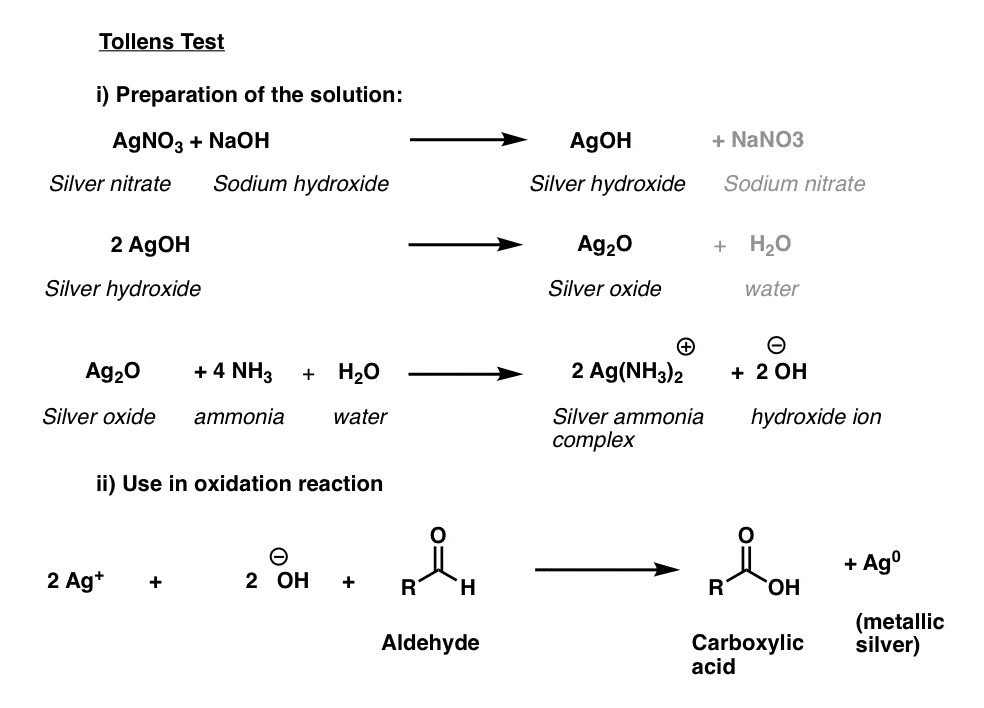
Tollens lösning
den aktiva ingrediensen i Tollens-testet, + , har inte lång hållbarhet och som Fehlings’ och Benedict-lösningarna är bäst beredda färska.
de tre första raderna nedan beskriver proceduren. Silvernitrat omvandlas till silverhydroxid, som bildar silver (i) oxid, Ag2O., Därefter resulterar tillsats av vattenhaltig ammoniak (NH3) i bildandet av silver-ammoniakkomplexet som är det aktiva oxidantet.
det prov som ska testas tillsätts sedan till det nyberedda aktiva oxidantet i en grundlösning. Ett positivt test resulterar i att en vacker spegel av silvermetall fälls ut på reaktionskärlet. (En variant av denna procedur används för framställning av speglar).
hur fungerar det?
det första att notera är att alla dessa procedurer förekommer i grundlösningen.
varför?, Det finns åtminstone två goda skäl till detta som vi kan prata om.
- för det första kan sura förhållanden hydrolysera eventuella acetaler som finns för hemiacetaler, vilket ger ett falskt positivt test.
- för det andra påskyndar basen avsevärt hastigheten för ringkedjans tautomerism (dvs. interkonvertering mellan den cykliska hemiacetalformen och den linjära aldehydformen).
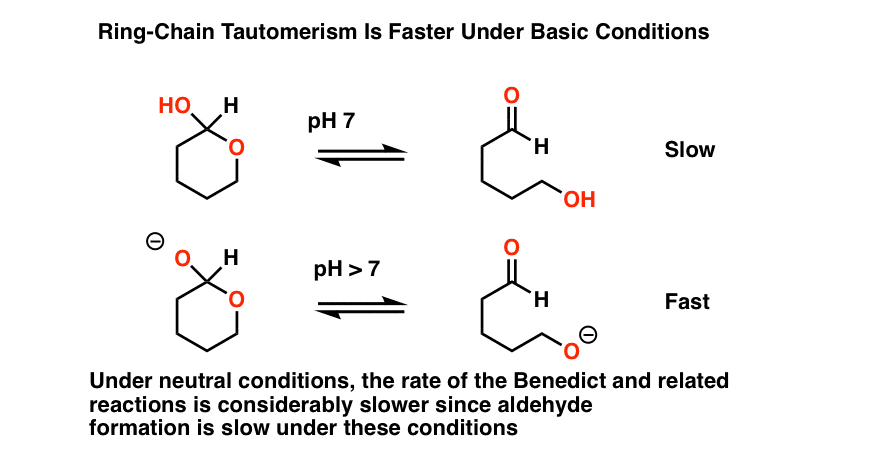
bottom line här är att adding base har effekten av att öka koncentrationen av startaldehyden.,
de mekanistiska detaljerna är skumma och du hittar dem inte i någon inledande lärobok
Jag kan inte hitta en enda instans av mekanismen för Fehlings eller Benedict lösningar belyses slutgiltigt online. Om jag har fel, berätta för mig (Lämna en kommentar).
det finns en tredje orsak till användningen av basen, även om jag inte är mycket angelägen om att prata om det. Du kanske märker att vi inte har nämnt mekanismerna för någon av dessa reaktioner. Det beror på att de exakta mekanismerna har varit svåra att belysa., Ett av de viktigaste stegen som är involverade i mekanismen för varje reaktion verkar vara en process som kallas ”single-electron transfer”, vilket är väsentligen när metallsaltet slurps en enda elektron av substratet, vilket skapar en friradikal och/eller karbocation.
en av åtkomstpunkterna för initiering av en enelektronöverföringsreaktion är en kolmetallbindning, som kan uppnås genom basfrämjande bildning av ett enolat.
som kräver att aldehyden har en proton på Alfa-kolet (dvs. vara ”enoliserbar”)., Det visar sig att Fehlings lösning gör ett skitjobb med testning för bensaldehyd, som saknar några protoner på Alfa-kolet och inte kan enoliseras. Således verkar det som om reaktionen måste fortsätta genom en enol.
Fehlings lösning oxiderar emellertid också formaldehyd till myrsyra och därmed till koldioxid, och denna process kan inte möjligen fortsätta genom en enol / enolatmediär.
så det är troligt att en mängd olika mekanistiska vägar kan vara i drift.
hur kan en mekanism se ut?
kanske, möjligen, något sådant här?,
håll muspekaren här för en popup-bild eller
om någon annan har en bättre idé, är du välkommen att kommentera nedan.
anmärkningar
bildkällor: Benedicts lösning. Fehlings lösning. Tollens test.
anmärkning 1. Detta är inte att säga att de är de mest praktiska metoderna för att förbereda karboxylsyror från aldehyder. När kemister vill förbereda en karboxylsyra från en aldehyd i gott utbyte, använder de inte någon av dessa tre processer. Det vanliga sättet att göra det är Pinnick oxidation.
Anmärkning 2., Det kvantitativa testet använder tydligen kaliumisocyanat, vilket resulterar i en färglös fällning.
Anm. 3: Det är troligt att enediol-intermediären faktiskt är den art som reagerar med Cu2 + i det inledande steget av mekanismen som leder till aldehyden. Se avsnittet mekanism.
anmärkning 4. En sak att notera: om sackaros upphettas med vattensyra före ett Fehlings/Benedict/Tollens-test, kommer ett positivt test att resultera., Det beror på att acetalbindningarna hydrolyseras av vattensyra för att producera de två ingående sockerarterna av sackaros (glukos och fruktos) som själva minskar sockerarter.
(avancerade) referenser och vidare läsning
- arten av Fehlings lösning
Thomas G. Hörner, Peter Klüfers
J. Inorg. Chem. 2016, 12, 1798-1807
DOI: 10.1002/ejic.201600168
även om reaktionsekvationen för Fehlings test kan se enkelt ut på papper, är de berörda arterna faktiskt ganska komplexa! - underkastelse av glutaraldehyd till Tollens-testet
William D., Hill
Journal of Chemical Education 1990, 67 (4), 329
DOI: 1021/ed067p329
Dialdehydes kommer också att ge en positiv Tollens test (silver spegel fällning). - Tollens test, fulminating silver och silver fulminate
Ian D. Jenkins
Journal of Chemical Education 1987, 64 (2), 164
DOI: 10.1021 / ed064p164
Tollens testet utförs vanligen i grundutbildningen organiska Kemi laboratorier, med noggrant testade förfaranden. Förfarandena måste vara robusta eftersom Tollensreagensen kan vara explosiv, vilket förklaras i denna anmärkning., - Fehling och Benedict tester
Ralph Daniels, Clyde C. Rush, och Ludwig Bauer
Journal of Chemical Education 1960, 37 (4), 205
DOI: 10.1021/ed037p205
Denna not är intressant eftersom författarna visar att Fehling och Benedict testerna är specifika för hemiacetaler, i reducerande socker – de misslyckas när de används med enkel alifatiska aldehyder. - En korrigering på Benedictus test
William D. Hill
Journal of Chemical Education 1982, 59 (4), 334
DOI: 10.,1021 / ed059p334
flera läroböcker använder Na2CO3 som bas i Benedict-testet, men enligt denna anteckning krävs NaOH för bildandet av Cu2