Polysilicates
La Orthosilicate Ion, SiO44-
La orthosilicate ion nu este prezent într-o mare varietate de minerale. Este o bază foarte puternică care nu va persista în soluție apoasă. În natură se găsește în combinație cu cationi acizi în săruri insolubile.
Polisilicate oligomerice
structurile de silicat polimeric necesită oxigeni de legătură (2-coordonate). Pentru a face loc unui oxigen de legătură, un oxid trebuie îndepărtat din siliciul „receptor”.
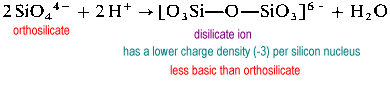
disilicat ion este mai puțin frecvente în natură., Se găsește numai în mineralul rar thortveitite, Sc2Si2O7. Structuri mai mari, cum ar fi trisilicat și tetrasilicat sunt extrem de rata.
Polisilicate oligomerice ciclice
în loc să formeze structuri cu lanț lung deschis, capetele lanțurilor vor lega eliminarea ionilor de oxid.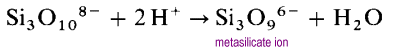
ionul metasilicat este un oligomer al ionului sio32 necunoscut. În aceste structuri, fiecare siliciu posedă doi atomi de punte și doi atomi de oxigen terminali. Există o densitate de încărcare de -2 pe atom de siliciu., Cele mai frecvente ciclic polysilicates sunt ciclice trimeri, (SiO3)36 – și ciclice hexamers (SiO3)612-.

trimer ciclic se găsește în minerale benitoite, BaTi(Si3O9.

Lanț Polysilicates
Liniare (1-D) polimeri de formula (SiO3)n2n – pot fi formate prin punți de oxigen. În aceste structuri există o încărcătură de -2 pe atom de siliciu., A group of minerals called the pyroxene minerals have this type of structure.
| |
|
| enstatite | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimene | LiAlSi2O6 |
| pollucite | CsAlSi2O6 |
Linear chains may be linked side-by-side if an oxide ion is replaced with another bridging oxygen atom., Dacă această legătură apare la supleant SiO3 grupuri în fiecare lanț, un dublu-structura lanțului (Si4O11)n6n – rezultate. În astfel de structuri există o reducere a încărcăturii și a numărului de atomi de oxigen pe atom de siliciu.
Crocidolitul, un mineral de azbest cu formula Na2Fe5 (OH)22, este un exemplu. Acest mineral este de natură fibroasă și are proprietăți rezistente la foc și căldură care rezultă din structura lanțului lung al anionului.
Sheet Polisilicates
când legarea laterală a lanțurilor este continuată la nesfârșit, mai mulți oxizi sunt eliminați și rezultă un polimer 2-D., Acești polimeri 2 – D se numesc silicați de foi și conțin anionul n4n. Mineralele care conțin această structură sunt ușor scindate în foi subțiri.,
china clay and vermiculite
3-D Polymeric Silicates
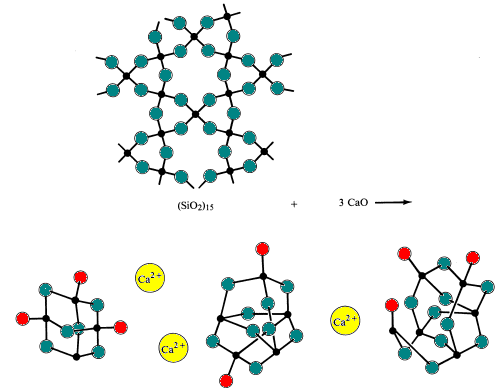
Sheets are linked into a 3-D polymer when all the oxide ions are eliminated (all oxygens in the structure are bridging)., Această structură conține oxid de silice n neîncărcat, care nu mai este bazic, ci mai degrabă un oxid acid. Multe minerale comune conțin această structură: cuarț, flint, jaspis, onix, ametist, citrin, agat și calcedonie.,
Succesive de polimerizare pașii de mai jos:
- Rezultat în reducerea succesivă a O/Si atom raport
- 4:1 în orthosilicate
- 2:1 în siliciu

 Loc următoarele minerale, în scopul de a crește gradul de polimerizare., Pentru a face acest lucru, calculați raportul O/Si (cu cât raportul este mai mic, cu atât structura este mai polimerizată.
Loc următoarele minerale, în scopul de a crește gradul de polimerizare., Pentru a face acest lucru, calculați raportul O/Si (cu cât raportul este mai mic, cu atât structura este mai polimerizată.
- pyrophyllite, Al2Si4O10(OH)2
- grunerite, Fe7Si8O22(OH)2
- spessartite, Mn3Al2Si3O12
- bustamite, și eu pot(SiO3)2
Geam
Când acid de siliciu reacționează cu bază de oxizi la temperaturi foarte ridicate (~1700 0C) și apoi s-a răcit prea repede pentru polisilicat de ioni pentru a permite fomation a ordonat polisilicat ioni găsit în minerale pentru a forma. Rezultatul este formarea unui solid amorf sau a unei sticle., Ochelarii se caracterizează prin faptul că nu au un punct de îngheț definit.
sticla simplă se face prin topirea (topirea) nisipului cu bicarbonat de sodiu și calcar (surse de oxizi de bază Na2O și CaO). În timpul acestui proces, punțile de siliciu-oxigen sunt rupte.
ochelari de Specialitate sunt realizate prin modificarea compoziția de acid și de bază de oxizi în sticlă.sticla Pyrex ™ este neobișnuit de rezistentă la șocul termic. Pentru a face 10-25% B2O3, un oxid acid, este încorporat în structură.,
Aflați mai multe despre ochelari de aici și de la Corning Museum Sticlă site-ul de Resurse.
Chimia Solului
faptul că din ce în ce mai polimerizat polisilicat ionilor de scăderea taxelor pe siliciu, care rezultă în a redus bazicitatea are importan consecințe în chimia solului.,cu cât este mai bazic anionul polisilicat al unui mineral, cu atât mai ușor va reacționa cu acizii slabi și va suferi intemperii.apa de ploaie este oarecum acidă datorită CO2 dizolvat chiar și în absența oxizilor de sulf și azot.
în timp, apa de ploaie va reacționa cu anionii de silicat mai puțin polimerixați pentru a înlocui ionii de oxid cu oxigenul de legătură, rezultând un silicat mai polimerizat. Oxizii sunt îndepărtați ca molecule de apă.,
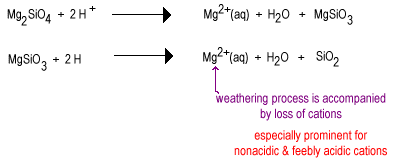
etapa intermediară de intemperii are cantități mari de silicați strat, cum ar fi argila, precum și unele cuarț. Aceste soluri tind să fie găsite în regiunile temperate sub o acoperire de iarbă sau copaci. Astfel de soluri sunt mai puțin fertile decât solurile dezertate recent irigate datorită pierderii nutrienților nonacidici ai plantei K+., Silicații de strat prezenți în solurile intermediare pot încă să dețină cationi pe suprafețele lor încărcate negativ, care pot fi eliberate pe măsură ce planta are nevoie de ele. Aceste soluri se găsesc în centurile de porumb și grâu încă destul de fertile.
substituția izomorfă
ionii Polisilicați au sarcini negative care trebuie contrabalansate de cationii corespunzători. Oxygenii terminali posedă suprafețe încărcate negativ care aproximează suprafețele apropiate de sarcină negativă., Cationii care sunt necesari pentru a neutraliza sarcina negativă a polisilicatului sunt localizați în straturile dintre lanțuri sau straturi sau în găurile tetraedrice sau octaedrice prezente în rețeaua 3-D.
tipurile de cationi găsite într-o anumită formă de polisilicat va depinde de”
- dimensiunea cationilor
- sarcina cationilor
deoarece există destul de multe seturi de ioni care au aceeași sarcină și raze foarte similare, există puține motive pentru unul dintre aceste tipuri potrivite de ioni să fie preferat față de altul atunci când un mineral este format pe răcirea magmei topite.,
De exemplu, olivina, care are o compoziție ideală de Mg2SiO4, poate contine diferite procente de isomorphous subtitution de Fe2+ (raza 92 pm) în loc de un număr egal de Mg2+ (raza 86 pm).
Primul Principiu al Isomorphous Subsititution
al Doilea Principiu de Isomorphous de Substituție
substituția Izomorfică crește numărul de substituții posibile în silicați.
Exemplecationii din majoritatea mineralelor de silicat sunt substituiți pe scară largă, ceea ce face ca minereurile neeconomice pentru majoritatea elementelor., Există relații diagonale ale elementelor (în special în a doua perioadă) cu elementele un grup la dreapta și o perioadă în jos pe masă.
 Care dintre următoarele minerale ar putea apărea de isomorphous substituirea proceselor în leucite, K(AlSi2O6)?,
Care dintre următoarele minerale ar putea apărea de isomorphous substituirea proceselor în leucite, K(AlSi2O6)?,
- K(YSi2O6)
- Rb(AlSi2O6)
- Ba(BeSi2O6)
- Ba(AlSi2O6)
INDICIU: Există două principii fundamentale de compuși ionici care trebuie să fie respectate în isomorphous de substituție:
- suma totală a tuturor cationilor trebuie să fie egală cu sarcina totală a tuturor anionilor.
- pentru ca substituția să fie izomorfă, numărul total de cationi care intră trebuie să fie aproximativ egal cu sarcina totală a tuturor cationilor înlocuiți.