Innledning
Corona-viruset SARS-CoV-2 har allerede spredt seg over hele verden og er for tiden, med ingen vaksine tilgjengelig ennå, ustoppelig. Pr. i dag COVID-19 påvirker mer enn 3,000,000 bekreftet pasienter globalt. Første linje medisiner er antivirale legemidler, og flere presserende kliniske studier er under veis., Men en fersk studie testing av HIV protease-inhibitor kombinasjon lopinavir og ritonavir viste ingen signifikante antiviral aktivitet mot SARS-CoV-2 i pasienter med alvorlig sykdom (1). Så lenge vi ikke har spesifikk antiviral behandling mot SARS-CoV-2, vi trenger å gi støttende symptomatisk behandling for å hindre lunge-svikt, den vanligste årsaken til COVID-19 dødelighet.,
Type II-Alveolar Celler Blir Skadet av SARS-COV-2
Viral infeksjon og resulterer alveolar celle ødeleggelse tiltrekke seg immun celler med en overdreven alveolar exudative og mellomliggende inflammatorisk reaksjon. En storm av cytokin og chemokine produksjon resultater i lungevev ødeleggelse og til slutt i alvorlig akutt respiratorisk distress syndrom (BOARDS). SARS-CoV-2 samt SARS-CoV inn i cellene gjennom angiotensin konvertering enzym reseptor 2 (ACE2)., ACE2 er sterkt uttrykt på apical overflaten av luftveiene epithelia, vaskulær endothelia, nyre-og hjerte-og vev samt diverse andre celler (2). Som de som går inn gjennom luftveiene, SARS-CoV, og SARS-CoV-2 kan spesielt ødelegge celler, som hovedsakelig uttrykke ACE2 reseptor på deres overflater, nemlig type II-alveolar-celler (2, 3).
Som progenitor celler for alveolar epitel, type II alveolar celler er «defender av alveolus» (4)., De har alveolar homeostase, spesielt etter mikrobiell lungeskade, hvor de kontrollerer inflammatorisk respons.
Gjennom sin produksjon av beskyttende lunge overflateaktivt stoff, type II alveolar celler redusere lunge overflatespenning og dermed legge til rette for pusting og gassutveksling, og i tillegg er sentrale for reparasjon prosesser etter traumer (5) (Figur 1). Skade på type II-alveolar celler drastisk reduserer pulmonal overflateaktivt middel produksjon og sekresjon å alveolar plass., Dette er etterfulgt av atelectasis på grunn av lunge overflateaktivt stoff dysfunksjon som ytterligere reduserer lunge compliance (6). Luft-væske-interphase er forskrekket i SARS-CoV-2 infiserte pasienter som fører til lungeskader. ACE2 seg selv beskytter mot lunge skade selv om anti-inflammatorisk og anti-fibrotic mekanismer. Derfor, bruk av rekombinant kalles angiotensin konvertering enzym (ACE) ville ikke bare blokkere virus reseptor binding nettsteder, men også gi lunge-beskyttelse. I scenario der SARS-CoV-2 binder seg til ACE2, beskyttende ACE bindende er sterkt redusert., Ødeleggelse av alveolar celler er etterfulgt av redusert blod oksygenering, lunge fibrose, ødem i bena, nedsatt regenerering, og til syvende og sist fører til respiratorisk svikt (7).
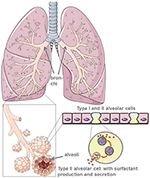
Figur 1. Modell av lunge-og alveolar morfologi. Lunge overflateaktivt stoff er produsert av type-II-alveolar celler. Opprettet ved hjelp av smart servier medisinsk art under https://creativecommons.org/licenses/by/3.0/.,
Lunge Overflateaktivt stoff som Beskyttende Anti-Inflammatorisk BOARDS Terapi
Respiratorisk svikt er også kjent fra en helt annen opprinnelse, nemlig i tidlig fødte spedbarn med redusert lunge overflateaktivt middel produksjon i forhold til sikt-født barn. Uten tilstrekkelig lunge overflateaktivt stoff, alveoler kollapse under utpust noe som resulterer i dårlig blod oksygenering.
Lunge overflater skildre luft-væske-interphase og er i konstant bevegelse under inn – og utpust. Sistnevnte gir risiko for vev sammenbrudd på grunn av væske overflatespenning., Lunge overvinner denne faren ved å dekke overflaten med lunge-overflateaktivt middel. Lunge overflateaktivt stoff er produsert i spesialiserte celler som finnes i terminalen lunge grener, type II alveolar celler, som begynne å produsere lunge overflateaktivt stoff umiddelbart etter fødsel (8).
Lunge overflateaktive stoffet er en blanding av fosfolipider og fire overflateaktivt stoff proteiner (SP), nemlig den hydrofile SP A og SP-D, også kalt collectins, og lipofile SP-B-og SP-C (9). Lunge overflateaktivt stoff senker overflatespenningen og dermed hindrer den alveolare kollapse under utpust., Alle SP bidra til det medfødte immunsystemet, i lunge, mens SP-B-og SP-C påvirke konsistens av phospholipid rik overflateaktivt stoff samt (10). Nylig, roman overflateaktivt middel assosiert proteiner (SFTA) ble beskrevet med lignende egenskaper i forhold til den «klassiske» SP (11-13). SFTA2 er hydrofile, og viser lignende egenskaper i forhold til SP A og SP-D (13). SFTA3 forbedrer phagocytosis av macrophage cellelinjer (14) og er en amfifile protein (12)., Derfor er det sannsynlig til å være til stede i de kommersielt tilgjengelige lipofile utdrag av dyr lungene og kan styrke phagocytotic aktivitet av makrofager mot CoV-2.
I tidlig fødte spedbarn, lunge overflateaktivt middel produksjon er ikke nok med dårlig blod oksygenering og høy alveolar overflatespenning fører til økt inflammatorisk reaksjon.
Starter i slutten av syttitallet, eksogene storfe eller svin lunge overflateaktivt stoff utvunnet fra bronkial lavage ble opprettet som en terapi for BOARDS hos premature barn., Behandling med lunge-surfaktant forberedelser fører til bedret oksygenering og økt overlevelse (15-17). Av notatet, behandling med naturlig forekommende lunge surfaktant hadde et bedre resultat med hensyn til spedbarn overlevelse i forhold til syntetiske lunge overflateaktivt stoff (17). Naturlig lunge tensider er en blanding av lipider (90%) og surfaktant proteiner (10%) som regulerer aktiviteten av alveolære makrofager og redusere betennelse. Den lipofile lunge overflateaktivt stoff brøkdel har anti-inflammatoriske egenskaper når den brukes intratracheally til lungene (18) samt lokalt på huden (19)., I hud, lunge overflateaktivt middel reduserer uttrykk for pro-inflammatorisk og pro-fibrotic gener i sår in vivo. I ulike in vitro og in vivo murin og menneskelige modeller av sår, betennelser, lunge overflateaktivt stoff redusert TNF-α, TACE og IL-6 (19), som er høyt opphøyet i alvorlig påvirket COVID-19 pasienter.
Nyere funn viser at SARS-CoV-2 medfører ødeleggelse av type II alveolar celler i COVID-19 forbundet lungebetennelse (2). Akkurat disse cellene produserer lunge overflateaktivt middel og hindre lunge kollaps., Videre, lymphocytopenia med massiv frigjøring av cytokiner er en annen faktor som fører til lunge-svikt og død i alvorlige tilfeller av COVID-19 pasienter. Derfor, anti-inflammatorisk mål, for eksempel anti-TNF-og anti-IL-6 har blitt foreslått for å bedre kontroll alvorlig COVID-19 infeksjon (20).,
Diskusjon: Bruk av Lunge Overflateaktivt middel for Pulmonal Barriere Restaurering hos Pasienter Med COVID-19 Lungebetennelse
Selv om lunge overflateaktivt stoff terapi er standard, veldig trygg og effektiv behandling for neonates med STANDARDER, behandling med rekombinant SP-C basert surfaktant ikke viser bedre overlevelse i store randomiserte kontrollerte studier hos voksne (18). Viktigere, bruk av naturlige overflateaktive stoffer synes å være en fordel i forhold til syntetiske tensider (16, 17) med betydelig forbedring i blodet oksygenering og kortere ventilasjon tid hos spedbarn (16)., Meconium aspirasjon syndrom ligner COVID-19 lungebetennelse med redusert overflateaktivt middel produksjon og destruksjon av type II alveolar celler (21). Tidlig administrasjon av naturlige lunge overflateaktivt stoff redusert ECMO behandling og ventilasjon tid (21). Dette tyder på at tidlig administrasjon av naturlige lunge overflateaktivt stoff kan faktisk forbedre lungefunksjonen også hos voksne pasienter med alvorlig BOARDS, mens årsaken til dødsfallet kan ikke være den kollapset lunge alene, men snarere en multi-organ svikt., I tillegg, ulike risikofaktorer for utvikling av STANDARDER og ulike phenotypes antyde mulige varierende effekter på grunn av terapeutiske tiltak. Dermed gunstige effektene av overflateaktivt stoff terapi i COVID-19 tilhørende STANDARDER pasienter er tenkelig, spesielt når den brukes tidlig i behandlingen strategi mot lunge-svikt.,
på Grunn av den robuste anti-inflammatorisk og lunge beskyttende effekt og dagens presserende behov for lunge støttende behandling, vi foreslår adjuvant behandling av COVID-19 lungebetennelse pasienter på ICUs med naturlig lunge tensider i tillegg til dagens standard av STANDARDER intensive care behandling. Nåværende tyder på at dette vil øke blod oksygenering, redusere lungeødem, og forbedre overdreven inflammatorisk reaksjon funnet i lunge obduksjoner av COVID-19 pasienter (22)., Windtree therapeutics™ kunngjorde sine planer om å teste KL4, et syntetisk overflateaktivt stoff, i alvorlige COVID-19 infiserte pasienter (https://www.windtreetx.com/). I Tyskland, Lyomark Pharma GmbH planlegger å teste sine naturlige multicomponent lunge overflateaktivt stoff bovactant i voksen COVID-19 pasienter med lungebetennelse som godt (www.lyomark.com).
Kommersielt tilgjengelig lunge overflateaktivt stoff er relativt billig for ICU standarder, lett tilgjengelig og har ingen kjente bivirkninger hos barn og voksne., Forsiktighet bør utvises hos pasienter med kjent allergi mot storfe eller svin produkter, som lunge tensider er stort sett høstet fra storfe (bovactant, Alveofact®) eller svin (poractant alfa, Curosurf®) lungene ved lavage eller vev mincing etterfulgt av utvinning av lipid brøkdel.
Administrasjon er enkelt ved å legge til den rekonstituerte lyophilizate i tracheal rør av ventilerte pasienten å levere stoffet direkte til alveolar plass. Med hensyn til bovactant, en forstøveren ble nylig godkjent for klinisk bruk i USA av FDA., Ved å dekke den ytre overflaten av alveoler, lunge overflateaktivt middel virker direkte på inflammatoriske celler å redusere cytokin produksjon og destruksjon av vevet. Dermed, det gjenoppretter pulmonal barrieren og dermed forhindrer lungene kollapser (Figur 2). Følgelig, det vil redusere varigheten av ventilasjon terapi, gjøre det lettere å puste, og dermed bidra til pasientenes recovery.
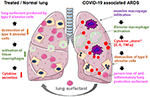
Figur 2. Hypotetisk mekanismen for eksternt påførte lunge overflateaktivt middel for pulmonal beskyttelse i alvorlige COVID-19 tilhørende STANDARDER., COVID-19 tilhørende STANDARDER er preget av massive macrophage infiltrasjon, vev alveolar macrophage aktivering og en potentiation av cytokin produksjon i lunge (cytokin «storm»), som fører til ødeleggelse av surfaktant å produsere type II-alveolar celler, noe som forverrer situasjonen gjennom tap av anti-inflammatorisk, anti-fibrotic lunge overflateaktivt middel. Eksogene overflateaktivt stoff kan redusere betennelse og dermed gjenopprette pulmonal overlevelse. Opprettet ved hjelp av smart servier medisinsk art under https://creativecommons.org/licenses/by/3.0/.,
Forfatter Bidrag
Alle forfatterne har bidratt til design, skrive og konseptualisering av manuskriptet. UM og KM redigert og utformet tallene.
interessekonflikt
forfatterne erklærer at forskningen ble utført i fravær av kommersielle eller finansielle forhold som kan oppfattes som en potensiell interessekonflikt.
Erkjennelsene
Vi vil gjerne takke Desiree Schumann (University of Basel) for hennes innsiktsfulle støtte i å skrive dette manuskriptet., Forfatterne er støttet av det tyske Research Foundation (DFG) og JDRF. Vi ønsker å be om unnskyldning for ikke siterer mange viktige publikasjoner på grunn av plassbegrensninger.
9. Bernhard W. Lunge overflateaktivt stoff: funksjon og sammensetning i sammenheng med utvikling og luftveier fysiologi. Ann Anat. (2016) 208:146-50. doi: 10.1016/j.aanat.2016.08.003
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
10. Wright JR., Den «visdom» lunge overflateaktivt stoff: balansering vert forsvar og overflatespenning å redusere funksjoner. Am J Physiol Lunge Cell Mol Physiol. (2006) 291:L847–50. doi: 10.1152/ajplung.00261.2006
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
11. Schicht M, Garreis F, Hartjen N, Beileke S, Jacobi C, Sahin A, et al. SFTA3 – en roman overflateaktivt middel protein av okulær overflate og sin rolle i hornhinnen sårheling og rive filmen overflatespenning. Sci Rep. (2018) 8:9791. doi: 10.,1038/s41598-018-28005-9
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Mittal RA, Hammel M, Schwarz J, Heschl KM, Bretschneider N, Flemmer AW, et al. SFTA2–a novel secretory peptide highly expressed in the lung–is modulated by lipopolysaccharide but not hyperoxia. PLoS ONE. (2012) 7:e40011. doi: 10.1371/journal.pone.0040011
PubMed Abstract | CrossRef Full Text | Google Scholar
15., Ramanathan R. Overflateaktivt stoff terapi i tidlig fødte spedbarn med respiratorisk distress syndrom og i nærheten-begrepet eller begrepet nyfødte med akutt RDS. J Perinatol. (2006) 26(Suppl. 1):S51–6; diskusjon S63-4. doi: 10.1038/sj.jp.7211474
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
16. Er JV, Zimmermann LJ. Hva er nytt i overflateaktivt stoff? En klinisk se på den siste utviklingen i neonatology og pediatri. Europ J Pediatri. (2007) 166:889-99. doi: 10.,1007/s00431-007-0501-4
PubMed Abstrakt | CrossRef Full Tekst | Google Scholar
17. Ainsworth SB, Beresford MW, Milligan DW, Shaw NJ, Matthews JN, Fenton AC, et al. Pumactant og poractant alfa for behandling av respiratorisk distress syndrom i neonates født på 25-29 ukers svangerskap: en randomisert studie. Lancet. (2000) 355:1387-92. doi: 10.,1016/S0140-6736(00)02136-X
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Spragg RG, Lewis JF, Walmrath HD, Johannigman J, Bellingan G, Laterre PF, et al. Effect of recombinant surfactant protein C-based surfactant on the acute respiratory distress syndrome. N Engl J Med. (2004) 351:884–92. doi: 10.1056/NEJMoa033181
PubMed Abstract | CrossRef Full Text | Google Scholar
21., Findlay RD, Taeusch HW, Walther FJ. Surfactant replacement therapy for meconium aspiration syndrome. Pediatrics. (1996) 97:48–52.
PubMed Abstract | Google Scholar