Transport av Karbondioksid i Blodet
karbondioksid molekyler som transporteres i blodet fra kroppen vev til lungene ved en av tre metoder: ved oppløsning direkte inn i blodet, binding til hemoglobin, eller bæres som en bicarbonate ion. Flere egenskaper av karbondioksid i blodet påvirker transporten. Første, karbondioksid er mer løselig i blodet enn oksygen., Om 5 til 7 prosent av alle karbondioksid er oppløst i plasma. Andre, karbondioksid kan binde seg til plasma proteiner eller kan gå inn i røde blodlegemer og binder seg til hemoglobin. Dette skjemaet tar om lag 10 prosent av karbondioksid. Når karbondioksid bindes til hemoglobin, et molekyl kalt carbaminohemoglobin er dannet. Binding av karbondioksid til hemoglobin er reversibel. Derfor, når den når lungene, karbondioksid kan fritt ta avstand fra hemoglobin og bli utvist fra kroppen.,
Tredje, de fleste av karbondioksid molekyler (85 prosent) er gjennomført som en del av bikarbonat buffer system. I dette systemet, karbondioksid diffunderer inn i de røde blodcellene. Karbonsyre anhydrase (CA) i de røde blodcellene raskt konverterer karbondioksid i syre, karbonsyre (H2CO3). Kullsyre er en ustabil middels molekyl som umiddelbart distanserer inn (HCO−3) og hydrogen (H+) ioner. Siden karbondioksid er raskt omgjort til bicarbonate ioner, denne reaksjonen gjør for å fortsette opptaket av karbondioksid i blodet ned sin konsentrasjon gradient., Det er også resulterer i produksjon av H+ – ioner. Hvis for mye H+ er produsert, det kan endre blodets pH. Imidlertid, hemoglobin binder seg til den frie H+ ioner og dermed begrenser endringer i pH. Den nylig syntetisert bicarbonate ion er transportert ut av røde blodlegemer inn i den flytende komponent av blod i bytte for en klorid ion – (Cl–); dette kalles
. Når blodet når lungene, bicarbonate ion er fraktet tilbake til den røde blodceller i bytte for klorid ion. H+ – ion-dissosierer fra hemoglobin og binder seg til bicarbonate ion., Dette produserer kullsyre mellomledd som er konvertert tilbake til karbondioksid gjennom enzymatisk action på CA. De karbondioksid er utvist gjennom lungene under utpust.
– >
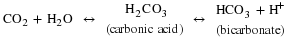
fordelen av bikarbonat buffer system er at karbondioksid er «gjennomvåt opp» i blodet med liten endring å pH i systemet. Dette er viktig fordi det tar bare en liten endring i den generelle pH i kroppen for alvorlig skade eller døden til følge., Tilstedeværelsen av denne bicarbonate buffer systemet gir også mulighet for folk til å reise og leve i store høyder: Når partialtrykket av oksygen og karbondioksid endre i store høyder, bicarbonate buffer-systemet justerer å regulere karbondioksid og samtidig opprettholde riktig pH i kroppen.
– >
kullosforgiftning
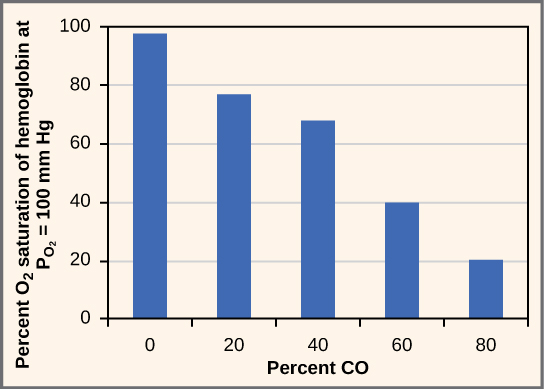
Mens karbondioksid lett kan assosiere og tar avstand fra hemoglobin, andre molekyler som for eksempel karbonmonoksid (CO) ikke kan. Karbonmonoksid har en høyere affinitet for hemoglobin enn oksygen., Derfor, når karbonmonoksid er til stede, det binder seg til hemoglobin fortrinnsvis over oksygen. Som et resultat, oksygen kan ikke binder seg til hemoglobin, så veldig lite oksygen blir transportert gjennom kroppen (Figur 20.22). Karbonmonoksid er en fargeløs, luktfri gass, og er derfor vanskelig å oppdage. Den er produsert av gassdrevne biler og verktøy. Karbonmonoksid kan forårsake hodepine, forvirring og kvalme; langvarig eksponering kan føre til hjerneskade eller død. Administrering av 100 prosent (ren) oksygen er den vanlige behandling for kullosforgiftning., Administrasjon av ren oksygen hastigheter opp separasjon av karbonmonoksid fra hemoglobin.
Oppsummering
Hemoglobin er et protein som finnes i røde blodceller som består av to alfa og to beta underenhetene som omgir en jern-holdige heme-gruppen. Oksygen lett binder dette heme-gruppen. Evnen til å binde oksygen øker mer oksygen molekyler som er bundet til heme., Sykdom stater og endrede forhold i kroppen kan påvirke bindingen evne til oksygen, og du vil øke eller redusere sin evne til å ta avstand fra hemoglobin.
karbondioksid kan bli transportert via blodet via tre metoder. Det er oppløst direkte i blodet, bundet til plasma proteiner eller hemoglobin, eller konverteres til bicarbonate. De fleste av karbondioksid er transportert som en del av bikarbonat system. Karbondioksid diffunderer inn i røde blodlegemer., Inne, karbonsyre anhydrase omdanner karbondioksid i syre, karbonsyre (H2CO3), som senere blir hydrolysert til bicarbonate (HCO−3) og H+. H+ – ion-binder seg til hemoglobin i røde blodlegemer, og bikarbonat er transportert ut av de røde blodcellene i bytte for en klorid ion. Dette kalles klorid skift. Bicarbonate forlater de røde blodcellene og går over i blodet plasma. I lungene, bikarbonat er fraktet tilbake til den røde blod celler i bytte for klorid., H+ dissosierer fra hemoglobin og kombinerer med bicarbonate å danne kullsyre med hjelp av karbonsyre anhydrase, noe som ytterligere catalyzes reaksjonen å konvertere kullsyre tilbake til karbondioksid og vann. Karbondioksid er deretter utvist fra lungene.
Øvelser
- nyrene er ansvarlig for å fjerne overskudd av H+ – ioner fra blodet. Hvis nyrene svikter, hva ville skje med blod pH og til hemoglobin affinitet for oksygen?
- Hvilken av de følgende IKKE vil lette overføringen av oksygen til vev?,
- redusert kroppstemperatur
- redusert pH i blodet
- økt karbondioksid
- økt mosjon
- De fleste av karbondioksid i blodet transporteres med ________.
- binding til hemoglobin
- oppløsning i blodet
- konvertering til bicarbonate
- binding til plasma proteiner
- De fleste av oksygen i blodet og transporteres med ________.,
- oppløsning i blodet
- blir gjennomført som bicarbonate ioner
- binding til blodet plasma
- binding til hemoglobin
- Hva ville skje hvis ingen karbonsyre anhydrase var til stede i røde blodlegemer?
- Hvordan gjør administrasjon av 100 prosent oksygen lagre en pasient fra kullosforgiftning? Hvorfor ville ikke gi karbondioksid arbeid?
Svar
- blodet pH vil synke og hemoglobin affinitet for oksygen vil reduseres.,
- En
- C
- D
- Uten karbonsyre anhydrase, karbondioksid ville ikke være hydrolysert inn kullsyre eller bikarbonat. Derfor, svært lite karbondioksid (bare 15 prosent) ville transporteres i blodet vekk fra vevet.
- karbonmonoksid har en høyere affinitet for hemoglobin enn oksygen. Dette betyr at karbonmonoksid vil fortrinnsvis binder seg til hemoglobin over oksygen. Administrasjon av 100 prosent oksygen er en effektiv terapi fordi på at konsentrasjon, oksygen vil fortrenge karbonmonoksid fra hemoglobin.