소개
코로나 바이러스 SAR-CoV-2 는 이미 주위에 확산 전체가 세계가 현재 없는 백신이 사용할 수 있는 멈출 수 있습니다. 현재 COVID-19 는 전 세계적으로 3,000,000 명 이상의 확인 된 환자에게 영향을 미칩니다. 첫 번째 라인 약물은 항 바이러스 약물이며 여러 긴급 임상 시험이 진행 중입니다., 그러나,hiv 프로테아제 억제제 조합 인 lopinavir 와 ritonavir 를 시험 한 최근의 임상 시험은 중증 질환 환자에서 SARS-CoV-2 에 대해 유의 한 항 바이러스 활성을 나타내지 않았다(1). 로 우리가 하지 않아 특정한 항바이러스 치료에 사스 CoV-2,우리가 필요한 지원을 제공하는 증상 치료를 방지하 폐 실패의 가장 일반적인 원인 COVID-19 사망.,
유형 II 폐포세포에 의해 손상되 SAR-COV-2
바이러스 감염의 결과로 폐포세포 파괴를 유치 면역 세포 과도한 폐 삼출성과 간질 염증 반응입니다. 사이토 카인 및 케모카인 생산의 폭풍은 폐 조직 파괴와 궁극적으로 심각한 급성 호흡 곤란 증후군(ARDS)을 초래합니다. SARS-CoV-2 뿐만 아니라 SARS-CoV 는 안지오텐신 전환 효소 수용체 2(ACE2)를 통해 세포에 들어갑니다., ACE2 는기도 상피,혈관 내피,신장 및 심혈관 조직뿐만 아니라 다양한 다른 세포(2)의 정점 표면에서 높게 발현됩니다. 그들이 입력한 호흡기를 통해,사스 CoV,와 SARS CoV-2 월 특히 세포를 파괴하는 주로 표현 ACE2 수용체에 그들의 표면,즉 유형 II 폐포세포(2,3).
폐포 상피의 전구 세포로서,II 형 폐포 세포는”폐포의 수호자”(4)이다., 그들은 특히 염증 반응을 조절하는 미생물 폐 손상 후 폐포 항상성을 유지합니다.
통해 생산의 보호 폐 계면활성제,type II 폐포세포를 줄이는 폐 표면 장력하고 따라서 호흡을 촉진하고 가스의 교환,그리고 이외에는 중앙 위한 수리 프로세스를 외상 후(5)(그림 1). II 형 폐포 세포의 손상은 폐 계면 활성제 생산과 폐포 공간으로의 분비를 크게 감소시킵니다., 이것은 폐 순응도를 더욱 감소시키는 폐 계면 활성제 기능 장애로 인한 무기폐가 뒤 따른다(6). 공기-액체-인터 페이즈는 폐 손상으로 이어지는 sars-CoV-2 감염된 환자에서 교란된다. ACE2 자체는 항 염증 및 항 섬유 성 메커니즘이지만 폐 손상으로부터 보호합니다. 따라서,재조합 안지오텐신 전환 효소(ACE)의 사용은 바이러스 수용체 결합 부위를 차단할뿐만 아니라 폐 보호를 제공 할 것이다. SARS-CoV-2 가 ACE2 에 결합하는 시나리오에서는 보호 ACE 바인딩이 심각하게 감소합니다., 폐포 세포의 파괴는 혈액 산소화 감소,폐 섬유증,부종,재생 장애가 뒤 따르며 궁극적으로 호흡 부전으로 이어진다(7).
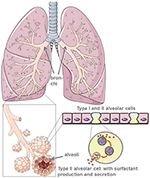
그림 1. 폐 및 폐포 형태의 모델. 폐 계면 활성제는 TYPE-II-폐포 세포에 의해 생성됩니다. https://creativecommons.org/licenses/by/3.0/에서 smart servier medical art 를 사용하여 만들었습니다.,
폐 계면활성제으로 방어적인 염증 ARDS 치료
호흡은 또한에서는 전혀 다른 원인을,즉 조산아와 감 폐 계면활성제는 생산 비교하는 용어 태어난 아이들입니다. 충분한 폐 계면 활성제가 없으면 호기 중에 폐포가 붕괴되어 혈액 산소가 잘 공급되지 않습니다.
폐 표면은 공기-액체-인터 페이즈를 묘사하며 인-및 호기 동안 일정한 움직임에 있습니다. 후자는 유체 표면 장력으로 인한 조직 붕괴의 위험을 부여합니다., 폐는 폐 계면 활성제로 표면을 덮음으로써 이러한 위험을 극복합니다. 폐 계면 활성제는 출생 직후 폐 계면 활성제를 생산하기 시작하는 말기 폐 가지 인 II 형 폐포 세포에서 발견되는 특수화 된 세포에서 생산됩니다(8).
폐 계면 활성제는 인지질과 4 개의 계면 활성제 단백질(SP),즉 콜렉 틴이라고도하는 친수성 SP-a 와 SP-D 와 친 유성 SP-B 와 SP-C(9)의 혼합물입니다. 폐 계면 활성제는 표면 장력을 낮추어 호기 중 폐포 붕괴를 방지합니다., 모든 SP 는 폐의 타고난 면역 반응에 기여하는 반면 SP-B 와 SP-C 는 인지질이 풍부한 계면 활성제의 일관성에도 영향을 미친다(10). 최근에,새로운 계면 활성제 관련 단백질(SFTA)은”고전적”SP(11-13)와 비교하여 유사한 성질로 기술되었다. SFTA2 는 친수성이며 SP-a 및 SP-D(13)와 비교하여 유사한 특성을 나타낸다. SFTA3 는 대 식세포 세포주(14)의 식균 작용을 향상시키고 양친 성 단백질(12)이다., 따라서 동물 폐의 상업적으로 이용 가능한 친 유성 추출물에 존재할 가능성이 있으며 CoV-2 에 대한 대 식세포의 식세포 활성을 향상시킬 수있다.
에 미숙아,폐 계면활성제 생산이 부족으로 가난한혈 산소화하고 높은 치조 표면장력을 선도하는 증가한 염증 반응입니다.
시대,외인 소 또는 돼지 폐 계면활성제에서 파생된 기관지 세척을 성공적으로 설립적으로 치료를 위해 호흡곤란 증후군에 미숙아., 폐 계면 활성제 제제로 치료하면 산소화가 강화되고 생존율이 증가합니다(15-17). 의 참고,치료를 자연적으로 발생하는 폐 계면활성제 더 나은 결과와 관련해 유아 생존에 비해성 폐 계면활성제(17). 천연 폐 계면 활성제는 지질(90%)과 계면 활성제 단백질(10%)의 혼합물로 폐포 대 식세포의 활성을 조절하고 염증을 감소시킵니다. 친 유성 폐 계면 활성제 분획은 피부(19)에 국소적으로뿐만 아니라 폐(18)에 내적으로 적용될 때 항 염증 특성을 갖는다., 피부에서 폐 계면 활성제는 생체 내 상처에서 친 염증성 및 친 섬유 성 유전자의 발현을 감소시킵니다. 에서 다양한 in vitro 및 in vivo murine 및 인간의 모델은 상처의 염증,폐 계면활성제 감소 TNF-α,TACE IL-6(19)는 매우 높은 심각하게 영향을 받 COVID-19 환자입니다.
최근 연구 결과에 따르면 SARS-CoV-2 는 COVID-19 관련 폐렴(2)에서 II 형 폐포 세포의 파괴를 유도합니다. 정확히 그 세포는 폐 계면 활성제를 생산하고 폐 붕괴를 예방합니다., 또한,사이토 카인의 다량 방출을 갖는 림프구 감소증은 COVID-19 환자의 심한 경우 폐 기능 부전 및 사망으로 이어지는 또 다른 요인이다. 따라서,항-TNF 및 항-IL-6 과 같은 항염증제 표적은 심각한 COVID-19 감염을보다 잘 통제하기 위해 제안되었다(20).,
토론의 사용:폐 계면활성제 폐 장벽을 회복을 가진 환자에서 COVID-19 폐
Although 폐 치료 계면활성제 표준입니다,매우 안전하고 효과적인 치료를 위한 신생아 ARDS,치료와 재조합 SP-C 기반으로는 계면활성제 보이지 않았다 향상된 생존에서 중요한 무작위 대조 임상 시험에서 성인(18). 중요한 것은,사용은 자연 계면활성제 유리한 것 같 비교를 합성계면활성제(16,17)에 상당한 개선으로혈 산소화하고 더 짧은 환기 시간에서 유아(16)., 메 코늄 흡인 증후군은 계면 활성제 생산이 감소하고 II 형 폐포 세포가 파괴 된 COVID-19 폐렴과 유사합니다(21). 천연 폐 계면 활성제의 조기 투여는 ECMO 치료 및 환기 시간을 감소시켰다(21). 이는 초반 관리의 자연 폐 계면활성제 수 있는 실제로 개선하는 폐 기능을 가진 성인 환자에서 심각한 ARDS,는 동안 죽음의 원인이 될 수 없습니다 붕괴 폐 혼자가 아니라 다중 기관의 실패입니다., 게다가,ARDS 및 상이한 표현형의 발달에 대한 상이한 위험 인자는 치료 조치로 인해 가능한 다양한 효과를 암시한다. 따라서,유익한 효과 계면활성제 치료에 COVID-19 관련 ARDS 환자들이 생각할 수 있는,특히 적용할 때 조기에 치료에 대한 전략 폐 실패입니다.,
기 때문에 강력한 염증 및 폐 방어 효능 및 오늘의 긴급한 필요를 위해 폐 치료 지원,우리가 제안의 보조 처리 COVID-19 폐렴을 환자에 중환자와 자연 폐 계면활성제에서는 또한 현재의 표준 ARDS 집중 치료. 현재 증거는 이것을 증가시킬 것입혈 산소화를 감소,폐 부종과 개선 과도한 염증 반응에서 발견 폐 부검의 COVID-19 환자(22)., Windtree therapeutics™는 심한 COVID-19 감염 환자(https://www.windtreetx.com/)에서 합성 계면 활성제 인 KL4 를 테스트 할 계획을 발표했습니다. 독일에서는 Lyomark Pharma GmbH 계획을 테스트하는 자신의 자연적인 깡통 폐 계면활성제 bovactant 성인 COVID-19 폐염을 가진 환자뿐만 아니라(www.lyomark.com).
상업적으로 사용할 수 있 폐 계면활성제 상대적으로 저렴한 ICU 기준,쉽게 사용할 수 없는 알려진 부작용에 어린이와 성인이다., 반드시 주의를 기울여야에서 환자들의 이미 알려진 알레르기에 대해 소 또는 돼지 제품으로 폐 계면활성제는 대부분에서 가을걷이 소(bovactant,Alveofact®)또는 돼지(poractant 알파,Curosurf®)폐하여 세척 또는 조직이 다음에 닦지의 추출 지질 부분이다.
관리는 단순한 추가하여 재구성 lyophilizate 으로 기관의 튜브를 통풍이 환자를 전달하는 약물을 직접 폐 공간입니다. Bovactant 와 관련하여 nebulizer 는 최근 FDA 에 의해 미국에서 임상 적으로 사용하도록 승인되었습니다., 폐포의 외부 표면을 덮음으로써 폐 계면 활성제는 사이토 카인 생성 및 조직 파괴를 감소시키는 염증 세포에 직접 작용합니다. 따라서 폐 장벽을 복원하여 폐 붕괴를 예방합니다(그림 2). 결과적으로 환기 요법의 지속 기간을 줄이고 호흡을 촉진하며 따라서 환자의 회복에 기여할 것입니다.
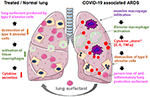
그림 2. 심한 COVID-19 관련 ARDS 에서 폐 보호를위한 외부 적용 폐 계면 활성제의 가설적인 메커니즘., COVID-19 관련 ARDS 특징으로 대규모의 세포 침윤,조직 폐 대식세포 활성화 및 potentiation 의 사이토카인 생산에서 폐암(cytokine”폭풍”),which 의 파괴에 이르게 생산 계면활성제 유형 II 폐포세포는 악화시키는 상황을 통해의 손실을 염증에 반대로 fibrotic 폐 계면활성제입니다. 외인성 계면 활성제는 염증을 감소시켜 폐 생존을 회복시킬 수 있습니다. https://creativecommons.org/licenses/by/3.0/에서 smart servier medical art 를 사용하여 만들었습니다.,
저자는 기여금
모든 저자는 기여하는 디자인,작문,개념의문입니다. UM 과 KM 는 수치를 편집하고 디자인했습니다.
이해의 충돌
저자가 선언하는 연구가 수행되었의 부재에서 어떠한 상업 또는 금융 서비스를 제공하는 것으로 해석될 수 있는 잠재적인 이해의 충돌.
감사
우리는 감사하는 데 지 슈만(바젤 대학)에 대한 그녀의 통찰력이 있는 지원서 작성이 원고., 저자는 독일 연구 재단(dfg)과 JDRF 의 지원을받습니다. 우리는 공간 제한으로 인해 많은 중요한 출판물을 인용하지 않은 것에 대해 사과하고 싶습니다.
9. Bernhard W.Lung 계면 활성제:발달 및 호흡 생리학의 맥락에서 기능 및 구성. 앤 아낫. (2016) 208:146–50. 도이:10.1016/j.aanat.2016.08.003
PubMed Abstract|CrossRef 전체 텍스트|Google Scholar
10. 라이트 주니어., 폐 계면 활성제의”지혜”:숙주 방어와 표면 장력 감소 기능의 균형. Am J Physiol 폐 세포 Mol Physiol. (2006)291:L847-50. 도이:10.1152/ajplung.00261.2006
PubMed Abstract|CrossRef 전체 텍스트/Google Scholar
11. Schicht M,Garreis F,Hartjen N,Beileke S,Jacobi C,Sahin A,외. SFTA3-안구 표면의 새로운 계면 활성제 단백질과 각막 상처 치유 및 눈물 막 표면 장력에서의 역할. Sci 의원(2018)8:9791. 도이:10.,1038/s41598-018-28005-9
PubMed Abstract | CrossRef Full Text | Google Scholar
13. Mittal RA, Hammel M, Schwarz J, Heschl KM, Bretschneider N, Flemmer AW, et al. SFTA2–a novel secretory peptide highly expressed in the lung–is modulated by lipopolysaccharide but not hyperoxia. PLoS ONE. (2012) 7:e40011. doi: 10.1371/journal.pone.0040011
PubMed Abstract | CrossRef Full Text | Google Scholar
15., Ramanathan R. 호흡 곤란 증후군이있는 조산아 및 급성 RDS 를 가진 단기 또는 장기 신생아에서 계면 활성제 치료. J Perinatol. (2006)26(Suppl. 1):S51–6;토론 S63-4. doi:10.1038/sj.jp.7211474
PubMed Abstract|CrossRef 전체 텍스트/Google Scholar
16. JV 되어,짐머만 LJ. 계면 활성제의 새로운 점은 무엇입니까? 신생아 및 소아과의 최근 발전에 대한 임상 적 견해. Europ J 소아과. (2007) 166:889–99. 도이:10.,1007/s00431-007-0501-4
PubMed Abstract|CrossRef 전체 텍스트|Google Scholar
17. Ainsworth SB,Beresford MW,Milligan DW,Shaw NJ,Matthews JN,Fenton AC,et al. 임신 25-29 주에 태어난 신생아의 호흡 곤란 증후군 치료를위한 Pumactant 및 poractant alfa:무작위 시험. 란셋. (2000) 355:1387–92. 도이:10.,1016/S0140-6736(00)02136-X
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Spragg RG, Lewis JF, Walmrath HD, Johannigman J, Bellingan G, Laterre PF, et al. Effect of recombinant surfactant protein C-based surfactant on the acute respiratory distress syndrome. N Engl J Med. (2004) 351:884–92. doi: 10.1056/NEJMoa033181
PubMed Abstract | CrossRef Full Text | Google Scholar
21., Findlay RD, Taeusch HW, Walther FJ. Surfactant replacement therapy for meconium aspiration syndrome. Pediatrics. (1996) 97:48–52.
PubMed Abstract | Google Scholar