Abstract
1928年、Alexander Fleming卿はロンドンの研究室でペニシリンの殺菌効果を観察した。 抗生物質:これは、今日の医学の最も重要な柱の一つの発見の最初のステップでした。 ペニシリンを大量に生産する方法を見つけるのに何年もかかり、大規模な生産は1945年まで始まりませんでした。, しかし、今日まで、フレミングは抗生物質の父と考えられており、彼の発見がなければ、細菌によって引き起こされる多くの感染症を治療することは することなく、抗生物質、少しでも感染した創傷が死亡する。 さらに、手術は抗生物質ではるかに安全であり、免疫システムが弱い人(子供や高齢者など)は細菌感染から容易に回復することができます。 しかし、細菌は抗生物質に耐性になりつつあり、これは1945年にフレミングがノーベル賞受賞演説の際に予測したものでもあった。,
小さな敵や友人
細菌は私たちにとって非常に重要です。 彼らは私たちと私たちの中に住んでおり、私たちは他の多くのものの中で、食品から特定の栄養素を得るためにそれらを使用しています(この若い心 しかし、病原体と呼ばれるいくつかの細菌も感染を引き起こし、いくつかの病原体は非常に危険です。 微生物の研究である微生物学の主要なテーマの一つである病原性細菌:肉眼では見ることができない小さな生命の形態。, 細菌が発見されて以来、微生物学者は同じ質問に直面してきました。 どのような細菌に感染し、人間を最も重要なことは、何ができ止めているのか。
個々の細菌は顕微鏡でしか見ることができません。 しかし、ほとんどの細菌は、栄養素がたくさんある環境でよく成長し、栄養素が非常に豊富なブイヨン(液体培地としても知られている)を使用して細菌, 無菌のブロスとその中の少数の細菌を含む試験管を一定の温度でインキュベートすると、液体は数時間で曇り、色が変わることさえあります。 ゼリーのような物質がブロスに加えられ、混合物がゼリーを溶かすために加熱されると、この物質はプレート(ペトリ皿としても知られている)に注がれて冷 細菌は、固体培地の表面上で培養することができる。 我々は十分な細菌を追加する場合、彼らは栄養豊富なゼリーの表面全体をカバーします。, 細菌が希釈され、プレート上に十分に広がっている場合、個々の細菌は、それが最終的に我々は細菌コロニーと呼ぶ肉眼で見える細菌の大きなグループを生成することをそんなに複製されます。 細菌の元のソースが複数のタイプを含んでいたら、異なった種類の細菌のコロニーは固体培地で育つかもしれません。 それらのコロニーの一つだけに触れて、その細菌を滅菌液体または固体培地に渡すと、一つのタイプの細菌しか含まない純粋な培養物を作ることができます。, 日常的に、微生物学者は、単一のタイプの細菌を用いた実験から明確な結論に達することができるように、純粋な培養物を用いて作業する。 しかし、それらの作業が滅菌状態で行われない場合、チューブおよびプレートは、他の細菌または環境に生息するいくつかの微視的な真菌によって汚染さ それが起こった場合、ほとんどの微生物学者はその文化を捨てて再び始めます。 しかしフレミングはほとんどの微生物学者とは異なっていた。
起こるのを待っている事故…
月曜日の朝、September3、1928、フレミングは家族の休日から戻ってきました。, 彼が休日に行く前に、フレミングは非常に一般的な病原体で働いていました:黄色ブドウ球菌。 フレミングは、これらの細菌が固体培地の表面に成長して、彼の研究室のベンチにいくつかのガラスのペトリ皿を残しました。 通常、これらのプレートは、他の実験でそれらを再利用するために実験技師によって滅菌される。 しかし、フレミングは、ベンチで数週間保管されたとしても、それらを破棄する前に、すべての実験を常に最後に見ていました(図1A)。 そのランダムにサンプルプルスタックからのプレートを見れば何でも興味深い事が起こにあります。, 彼の研究室は非常に原始的であったため、フレミングは一般的に環境からの酵母やカビによって引き起こされた彼のプレート上の汚染を持ってい しかし、一つのプレートは非常に異なって見え、彼はそのプレートに気づいたとき、彼は有名に言った”それは面白いです…。”プレートには細菌の密な培養物が接種されていましたが、それはまた、プレートの側面に大きなコロニーを作り出した顕微鏡の真菌で汚染されていました。 珍しかったことは、細菌が真菌コロニーに近い領域で増殖することができなかったということでした。, 細菌が完全に含まれていなかった真菌の周囲には完全に目に見える領域がありましたが、今日ではこれを阻害ゾーンと呼んでいます(図1B)。 したがって、フレミングは、真菌(Penicillium notatum)が危険な病原体である黄色ブドウ球菌を殺すものを生産していることを発見しました。 フレミングは抗生物質を発見したばかりで、最初はこれを”カビジュース”と呼んでいました。
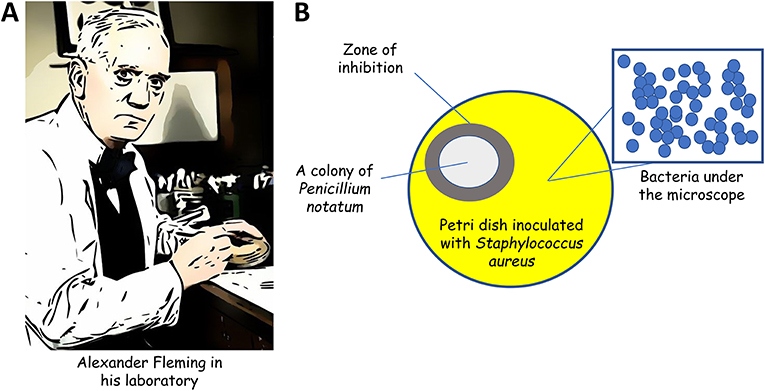
- 図1-(A)ロンドンの彼の研究室のベンチでサー*アレクサンダー*フレミング(1943)。,
- (B)Flemingは、真菌(Penicillum notatum)のコロニーが、危険な細菌病原体であるs.aureusを接種したペトリ皿を汚染していることを観察した。 興味深いことに、s.aureusはP.notatumのコロニー周辺地域で成長することができませんでした。 フレミングは、真菌が阻害ゾーンで黄色ブドウ球菌を殺す何かを生産していたと推測した。,
当時、フレミングも彼の同僚も、この発見は本当の重要性を持つことができるとは思わず、実際の重要性は十年以上後に実証されました。 しかし、フレミングはちょうど栄養素が豊富な環境で宇宙のために戦っている異なる微生物の間に存在する生物戦争を発見しました。 フレミングはペニシリンを作らなかった、彼は顕微鏡の真菌のコロニーがほとんど捨てられたプレート上の栄養素のために細菌と競合する方法としてペニシリンを生産することを観察した。, それ以来、微生物学者は、他の微生物が抗生物質を産生できるかどうかをテストするために、新しい抗生物質を自然界で検索し、このアプローチは非常に 新しい抗菌物質が同定されると、その物質は精製され、新しい抗生物質を大量に産生しやすくするため、または元の物質の新しいバージョンを作成するために化学的に修飾することができる。 私たちはまだ新しい抗生物質を探しており、”綿棒と送信”のような取り組みを通じて誰もがこれに参加することができます。
ペニシリンはどのように働くのですか?,
ペニシリンが細菌の増殖を阻害する方法は、1980年まで理解されていませんでした。 今私達はペニシリンがほとんどの細菌が彼らのセルを覆う壁を作成することができるように必要であるペニシリン結合蛋白質(PBPs)と呼出される細菌のある特定の酵素の活動を禁じることを知っています。 その壁がなければ、細菌細胞は環境にはるかに露出しており、環境が変化すると非常に簡単に死ぬことがあります。 ペニシリンの存在下では、細菌は自分自身を保護するためにこの細胞壁を産生することができず、そして彼らは死ぬ。, ペニシリンはβ-ラクタムと呼ばれる同様の抗生物質のファミリーの一部であり、多くの細菌は、これらの抗生物質を分解する酵素を産生するか、ペニシリンにもう結合しないPBPsの改変されたバージョンを取得することによってβ-ラクタムに耐性を持つようになる。
抵抗が上昇している…
フレミングが1945年にノーベル賞を受け入れた演説の中で予測したのは、細菌が抗生物質に耐性になる可能性があるということでした。 なぜなら、細菌は成長を制限するあらゆるハードルを克服するために非常に迅速に適応することができるからです。, 細菌が適応するのを助ける変化は、DNAのランダムな突然変異によって引き起こされる可能性があり、プロセスは本当に速いです—あなたはほとんど . さらに、抗生物質を産生する微生物の多くはまた、それらをそれらの抗生物質に対して耐性にする遺伝子を有する。 細菌は、新しい能力を得るために、他の生物からDNAを取得するのに非常に優れています。 これは水平遺伝子導入と呼ばれています。 病原性細菌が特定の抗生物質に耐性を持たせるために遺伝子を獲得すると、その抗生物質は診療所では役に立たなくなります。, の予防薬剤耐性、抗生物質用のものをご使用くださいが必要である(例えば、ウイルスできないによって殺される抗生物質となるようにすることができないためにウイルス感染症の正しい用法-用量の使用でも低いの量があり、新耐性菌)、または抗生物質の全てが定められており、必殺の原因菌の感染症です。 これらの措置を講じなければ、抗生物質耐性の広がりを助けている可能性があり、これは大きな問題です。, 実際、最も危険な細菌性病原体は、多くの抗生物質に耐性になっています。 薬剤の製造会社は抗生の抵抗が育つと同時にこれらの薬剤が有益でないかもしれないので新しい抗生物質の開発の興味を失っています。 したがって、新しい抗生物質が発見される速度は、新しい抗生物質耐性病原体の出現に対処するのに十分な速さではない。 私たちはすぐに細菌に感染した人々を効果的に治療することができなかった抗生物質以前の時代に戻るかもしれません。,
結論
ペニシリンの発見は、汚染が一般的であった実験室でのみ可能であった。 チャンスは確かに最初の抗生物質の発見に役割を果たしましたが、フレミングの訓練と実験室の練習は、彼が人類史上最も重要な薬の一つを特定するために不可欠でした。 残念なことに、抗生物質耐性のために、微生物学者は、感染症を治療する新しい方法を見つけるために細菌病原体との競争にあります。, 今日、私たちは病原体が宿主とどのように相互作用するか、抗菌剤がどのように機能するか、抗生物質耐性のメカニズムが何であるかについてより しかし、ペニシリンの発見後90年でさえ、現在の抗生物質危機と戦うために必要な作業はまだまだあります。 これに参加することで、綿棒とSendイニシアチブに参加することができます!
用語集
病原体:体に侵入し、感染を引き起こす微生物。
ペトリ皿:生きた細胞を培養するために使用される蓋付きのガラスまたはプラスチック製の皿。,
細菌コロニー:肉眼で見える固体培地の表面上で一緒に成長する細菌細胞のグループ。
阻害ゾーン:細菌コロニーが増殖しない抗生物質の供給源を取り巻く領域。
利益相反
著者は、この研究は、潜在的な利益相反と解釈され得る商業的または財務的関係がない場合に行われたと宣言している。
Madigan,T.M.,Bender,K.S.,Buckley,D.H.,Sattley,W.M.,and Stahl,D.a.2018. 微生物のブロック生物学。 第15回エドニー, ロンドン:ピアソン。
ブラウン、K.2017。 ペニシリンマン、アレクサンダー-フレミングと抗生物質革命。 チェルトナム:歴史プレス。
綿棒とイニシアチブを送信します。 オンラインで入手できます:https://www.lstmed.ac.uk/public-engagement/swab-send