Polisilicatos
el Ion ortosilicato, sio44 –
el ion ortosilicato no está presente en una amplia variedad de minerales. Es una base muy fuerte que no persistirá en solución acuosa. En la naturaleza se encuentra en combinación con cationes ácidos en sales insolubles.
Polisilicatos oligoméricos
las estructuras poliméricas de silicato requieren oxígenos puente (2-coordenada). Con el fin de hacer espacio para un puente de oxígeno, un óxido debe ser eliminado del silicio «receptor».
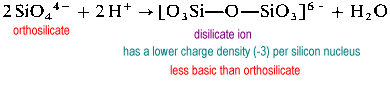
El disilicato de iones es poco común en la naturaleza., Se encuentra solo en el raro mineral thortveitite, Sc2Si2O7. Las estructuras más grandes, como el trisilicato y el tetrasilicato, son extremadamente rápidas.
Polisilicatos oligoméricos cíclicos
en lugar de formar estructuras largas de cadena abierta, los extremos de las cadenas se unirán eliminando los iones de óxido.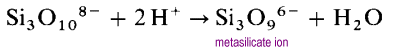
El ion metasilicato es un oligómero del desconocido ion SiO32. En estas estructuras cada silicio posee dos átomos de puente y dos átomos de oxígeno terminales. Hay una densidad de carga de -2 por átomo de silicio., Los polisilicatos cíclicos más comunes son los trímeros cíclicos, (SiO3)36 – y los hexámeros cíclicos (SiO3)612-.

El trímero cíclico se encuentra en el mineral benitoite, BaTi(Si3O9.

Polisilicatos de cadena
polímeros lineales (1-D) de Fórmula (SiO3)n2n – se puede formar a través de oxígenos puente. En estas estructuras hay una carga de -2 por átomo de silicio., A group of minerals called the pyroxene minerals have this type of structure.
| |
|
| enstatite | MgSiO3 |
| diopsite | CaMgSi2O6 |
| spodimene | LiAlSi2O6 |
| pollucite | CsAlSi2O6 |
Linear chains may be linked side-by-side if an oxide ion is replaced with another bridging oxygen atom., Si este enlace ocurre en grupos SiO3 alternativos en cada cadena, se obtiene una estructura de cadena doble (Si4O11)n6n. En tales estructuras hay una reducción en la carga y el número de átomos de oxígeno por átomo de silicio.la crocidolita, un mineral de asbesto de Fórmula Na2Fe5 (OH) 22, es un ejemplo. Este mineral es de naturaleza fibrosa y tiene propiedades resistentes al fuego y al calor que se deriva de la estructura de cadena larga del anión.
Polisilicatos de hoja
cuando el enlace de lado a lado de las cadenas se continúa indefinidamente, se eliminan más óxidos y se obtiene un polímero 2-D., Estos polímeros 2-D se llaman silicatos de hoja y contienen el anión n4n. Los minerales que contienen esta estructura se rompen fácilmente en láminas delgadas.,
china clay and vermiculite
3-D Polymeric Silicates
Sheets are linked into a 3-D polymer when all the oxide ions are eliminated (all oxygens in the structure are bridging)., Esta estructura contiene óxido de sílice n sin carga que ya no es básico, sino más bien un óxido ácido. Muchos minerales comunes contienen esta estructura: cuarzo, sílex, jaspe, Onix, amatista, Citrino, Ágata y calcedonia.,
Sucesivos polimerización por pasos:
- Resultado de las sucesivas reducción de S/Si átomo ratio
- 4:1 en orthosilicate
- 2:1 en sílice

 Coloque los siguientes minerales con el fin de aumentar el grado de polimerización., Para hacer esto, calcule la relación O/Si (cuanto menor sea la relación, más polimerizada será la estructura.
Coloque los siguientes minerales con el fin de aumentar el grado de polimerización., Para hacer esto, calcule la relación O/Si (cuanto menor sea la relación, más polimerizada será la estructura.
- pirofilita, al2si4o10(OH)2
- grunerita, Fe7Si8O22(OH)2
- spessartita, Mn3Al2Si3O12
- bustamita, CaMn(SiO3)2
vidrio
cuando la sílice ácida reacciona con óxidos básicos a temperaturas muy altas (~1700 0C) y luego se enfría demasiado rápido para que los iones de polisilicato permitan la formación de los iones de polisilicato ordenados que se encuentran en los minerales. El resultado es la formación de un sólido amorfo o vidrio., Las gafas se caracterizan por no tener un punto de congelación definido.el vidrio Simple se fabrica fundiendo (fusionando) arena con bicarbonato de sodio y piedra caliza (fuentes de los óxidos básicos Na2O y CaO). Durante este proceso, los puentes silicio-oxígeno se rompen.
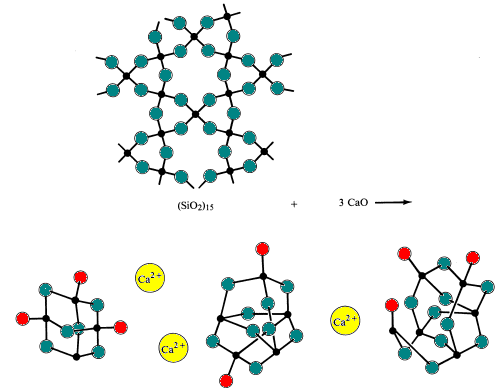
vidrios especiales, se hace mediante la alteración de la composición de ácidos y óxidos básicos en el vaso.
- El vidrio Pyrex ™ es inusualmente resistente al choque térmico. Para que sea 10-25% B2O3, un óxido ácido, se incorpora a la estructura.,
- Las gafas de color incorporan óxidos metálicos D-block como parte del componente básico de óxido
- La incorporación de óxido de estroncio da un vidrio que absorbe los rayos x emitidos por los televisores de color
- las finas cualidades ópticas necesarias en las lentes de las cámaras se pueden obtener mediante la incorporación de La2O3
Más información sobre las gafas aquí y en el sitio de recursos de vidrio del Museo Corning.
química del suelo
el hecho de que los iones de polisilicato cada vez más polimerizados tengan cargas decrecientes por silicio, lo que resulta en una basicidad reducida, tiene importantes consecuencias en la química del suelo.,
cuanto más básico sea el anión polisilicato de un mineral, más fácilmente reaccionará con ácidos débiles y se someterá a la intemperie.
El Agua de lluvia es algo ácida debido al CO2 disuelto incluso en ausencia de azufre y óxidos de nitrógeno. con el tiempo, el agua de lluvia reaccionará con los aniones de silicato menos polimerizados para reemplazar los iones de óxido con oxígeno puente produciendo un silicato más polimerizado. Los óxidos se eliminan como moléculas de agua.,
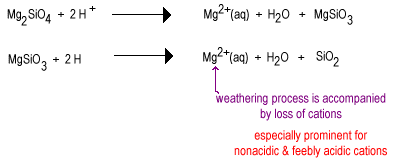
la etapa intermedia de la intemperie tiene grandes cantidades de silicatos de capa como arcilla, así como algo de cuarzo. Estos suelos tienden a encontrarse en regiones templadas bajo una cubierta de hierba o árboles. Tales suelos son menos fértiles que los suelos deser recién irrigados debido a la pérdida del nutriente vegetal no ácido K+., Los silicatos de capa presentes en suelos intermedios todavía pueden mantener cationes en sus superficies cargadas negativamente que pueden liberarse cuando las plantas los necesiten. Estos suelos se encuentran en los cinturones de maíz y trigo todavía bastante fértiles.
sustitución isomorfa
los iones de polisilicato tienen cargas negativas que deben ser contrarrestadas por cationes apropiados. Los oxígenos terminales poseen superficies cargadas negativamente que se aproximan a superficies compactas de carga negativa., Los cationes que se necesitan para neutralizar la carga negativa del polisilicato se encuentran en las capas entre las cadenas o capas o en los agujeros tetraédricos u octaédricos presentes en la red 3-D.
los tipos de cationes encontrados en una forma particular de polisilicato dependerán de»
- El tamaño de los cationes
- La carga de los cationes
dado que existen bastantes conjuntos de iones que tienen la misma carga y radios muy similares, hay poca razón para que uno de estos tipos coincidentes de iones se prefiera sobre otro cuando se forma un mineral en el enfriamiento del magma fundido.,por ejemplo, el olivino, que tiene una composición ideal de Mg2SiO4, puede contener porcentajes variables de substitución isomorfa de Fe2+ (Radio 92 pm) en lugar de un número igual de iones Mg2+ (radio 86 pm).
primer principio de substitución isomorfa
segundo principio de sustitución isomorfa
 Cual de los siguientes minerales podrían surgir por la sustitución isomorfa procesos en leucite, K(AlSi2O6)?,
Cual de los siguientes minerales podrían surgir por la sustitución isomorfa procesos en leucite, K(AlSi2O6)?,
- K(YSi2O6)
- Rb(AlSi2O6)
- Ba(BeSi2O6)
- Ba(AlSi2O6)
SUGERENCIA: Hay dos principios fundamentales de los compuestos iónicos que deben ser observadas en la sustitución isomorfa:
- La carga total de todos los cationes debe ser igual a la carga total de todos los aniones.
- para que la sustitución sea isomorfa, el número total de cationes va en el debe ser aproximadamente igual a la carga total de todos los cationes de ser reemplazado.