E E Z notação para alcenos
tabela de conteúdos
- Quando usamos cis– e trans– Notação em anéis?
- cis– and trans– Isomerism In Alkenes
- Cuidado com nomes ambíguos quando isomerismo geométrico é possível!,
- When “cis”- and “trans” fails: E and Z Notation
- Breaking Ties: The Method of Dots
- Conclusion: E and Z Notation For Alkenes
- Notes
- Quiz Yourself!
cis– and trans– isomerism in cyclic alcenes
E and Z Notation For Alkenes
This post was co-authored with Matt Pierce of Organic Chemistry Solutions. Pergunte ao Matt sobre agendar uma sessão de explicações online aqui.,
Revisão Rápida: cis– E trans – Isomerism (“Geométrica Isomerism”) Em Anéis
Anteriormente em nosso MOC série cycloalkanes, vimos que uma característica chave de pequenos anéis é que eles não podem ser transformados “de dentro para fora”, sem quebrar laços.
uma das consequências mais importantes disto é que pode levar à existência de estereoisómeros – moléculas que partilham a mesma fórmula molecular e a mesma conectividade, mas têm um arranjo diferente de átomos no espaço.
estas duas versões de 1,2 diclorociclopentano (abaixo) são um exemplo., Eles têm a mesma conectividade – ambos são 1,2-diclorociclopentano-mas têm diferentes arranjos de seus átomos no espaço. As clorinas estão no mesmo lado do anel no isômero da mão esquerda (ambas “cunhas”, saindo da página) e nos lados opostos (um entalado, um tracejado) no isômero da mão direita.
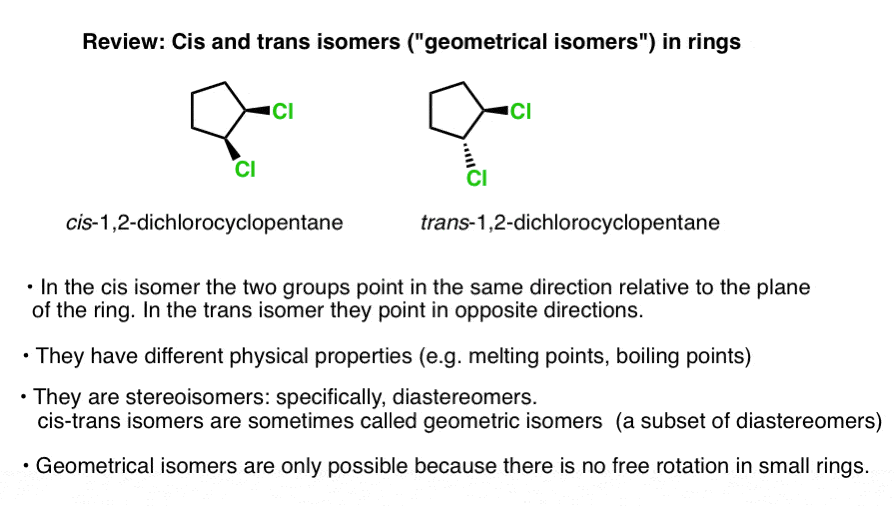
estas duas moléculas não podem ser interconvertidas através da rotação da ligação C-C sem ruptura do anel (use um kit modelo e tente, se preferir). São, portanto, isómeros.,moléculas que têm a mesma conectividade mas arranjo diferente no espaço são conhecidas como estereoisômeros.
especificamente, a relação entre as duas moléculas acima é a de diastereômeros: estereoisômeros que não são imagens espelhadas um do outro.estas duas moléculas têm propriedades físicas diferentes-pontos de ebulição diferentes, pontos de fusão, reactividades, características espectrais, etc.
1. Quando usamos cis – e trans-Notação em anéis?,
usamos os Termos cis-e trans-para denotar a configuração relativa de dois grupos um para o outro em situações onde há rotação restrita.
na nomenclatura, ” cis ” é utilizado para distinguir o isómero em que dois grupos idênticos (por exemplo, as duas clorinas em 1,2-diclorociclopentano) apontam na mesma direcção do plano do anel, e trans para distinguir o isómero em que apontam em direcções opostas.
um nome comum para estes isômeros chamados ” cis-trans “é”isômeros geométricos”.,
para o cis – trans – isomerism a existir em anéis, precisamos de duas condições:
- dois (e apenas dois) carbonos cada um com o não-idêntico substituintes acima e abaixo do anel
- os dois carbonos têm pelo menos um desses substituintes em comum
Em 1,2-dichlorocyclopentane vimos que C-1 e C-2 cada um tinha não-idênticos substituintes (H e Cl) acima e abaixo do anel, e cada um tinha pelo menos um substituinte em comum (na verdade, eles têm dois substituintes em comum: H e Cl ).
Aqui está outro exemplo: cis– e trans-1-etil-2-metilciclobutano., Note que cada um deles tem dois carbonos que cada um tem substituintes não idênticos acima e abaixo do anel (H E CH3; H E CH2CH3). Eles também têm pelo menos um substituinte em comum (H). Então podemos nos referir ao cis-1-etil-2-metilciclo-hexano como o isômero onde os dois hidrogenos estão apontando na mesma direção, e trans onde apontam em direções opostas.
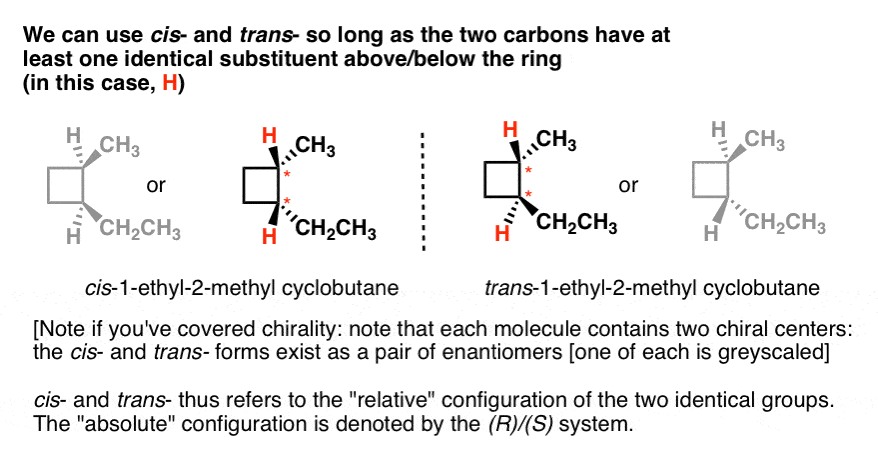
Se você cobriu a quiralidade, você também pode notar um fato interessante: existem duas maneiras de desenhar cada um dos isômeros cis e trans, e eles não podem ser sobrepostos um no outro., Estes são enantiômeros, a propósito.
assim cis-e trans-não especifica qual enantiômero (ele pode ser aplicado a qualquer um). Está apenas descrevendo a configuração relativa dos dois grupos (H neste caso). Se queremos especificar um enantiômero em particular, precisamos usar o sistema Cahn-Ingold-Prelog (CIP) de atribuir configurações R E S, que nos fornece a configuração “absoluta”. Nesse caso, cis e trans são redundantes.
porque cis-e trans-é relativo, não funciona se os dois carbonos não compartilham um substituinte comum. Nesse caso, você também tem que usar (R)/(s) .,
Estamos levando muito tempo para passar por anéis aqui, então vamos apenas ilustrar 2 exemplos onde ” cis “e trans” não funcionam em anéis e deixá-lo lá.
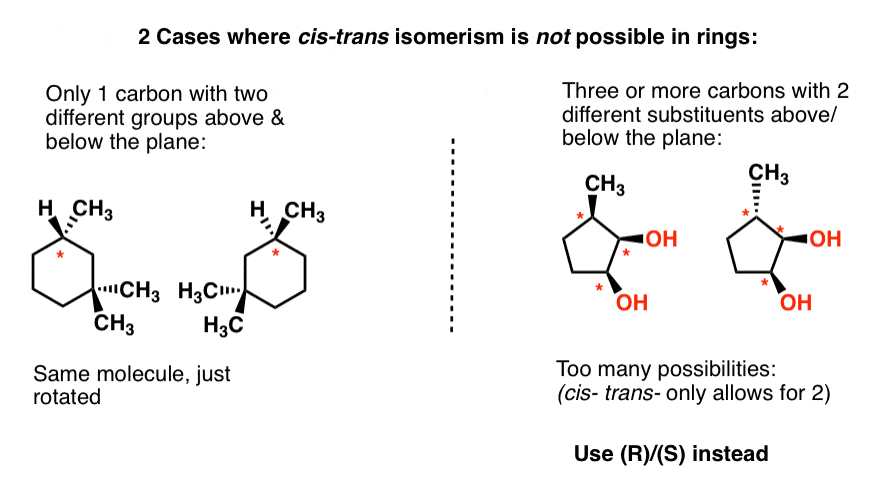
2. isomerismo cis e trans (isomerismo geométrico) em alcenos
isomerismo cis-trans também é possível para alcenos. Como em pequenos anéis, a rotação sobre ligações pi também é restringida: devido à sobreposição” lateral ” das ligações pi, não se pode rodar uma ligação pi sem quebrá-la., Isto está em contraste com as ligações sigma convencionais (ligações únicas) em moléculas acíclicas, onde a rotação livre é possível: testemunha 1,2-dicloroetano (abaixo da esquerda).portanto, podemos ter moléculas como cis-1,2-dicloroeteno e trans-1,2-dicloroeteno que podem ser separadas umas das outras devido às suas diferentes propriedades físicas.
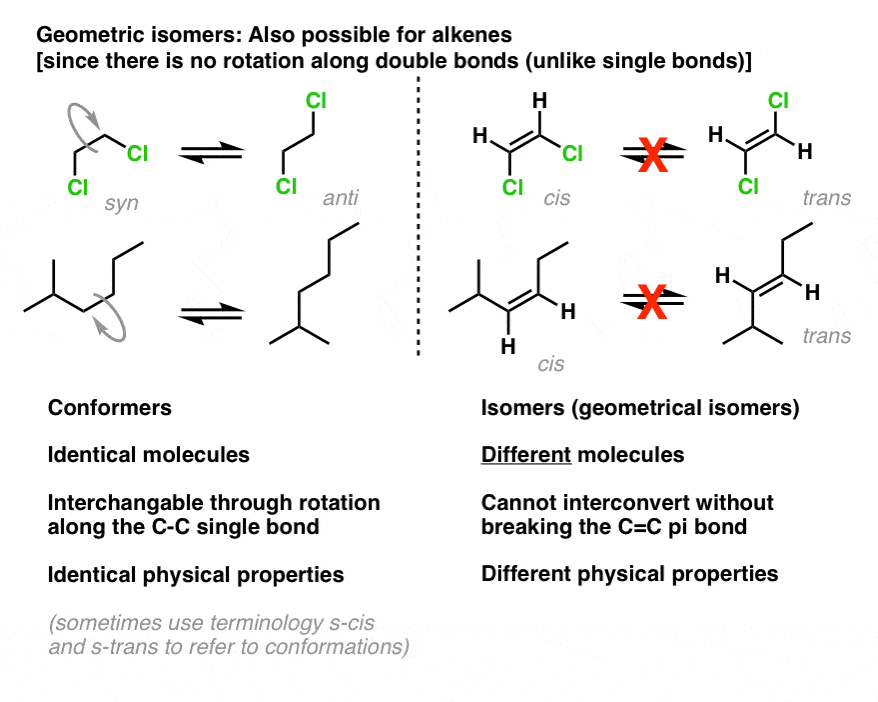
Podemos também utilizar a nomenclatura cis–trans para distinguir isómeros como o 2-metil-3-hexeno (acima da direita)., No isômero cis, os dois hidrogênios estão no mesmo lado da ligação pi, e no isômero trans, os dois hidrogênios estão no lado oposto da ligação.
Como com anéis, O requisito mínimo para o isomerismo cis-trans em alcenos é que cada carbono é ligado a dois grupos diferentes, e que os dois carbonos têm pelo menos um substituinte em comum. como com anéis, O isomerismo cis-trans não é possível se um dos carbonos da dupla ligação estiver ligado a dois grupos idênticos, como com 1,1-dibromo-1-propeno, abaixo. Tente você mesmo se não estiver convencido.,
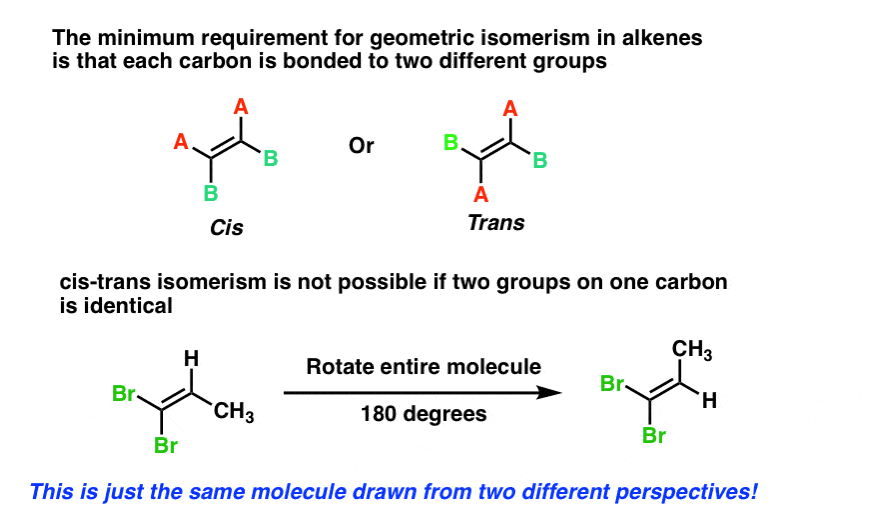
3. Cuidado com nomes ambíguos onde o isomerismo cis / Trans é possível
uma digressão rápida: uma consequência da nossa nova apreciação do isomerismo geométrico é que muitos nomes simples de moléculas são na verdade ambíguos.
Por exemplo, o descritor “3-hexeno” não descreve inequivocamente uma molécula específica. . Para determinar a molécula específica, precisamos especificar cis– ou trans– 3-hexeno.,
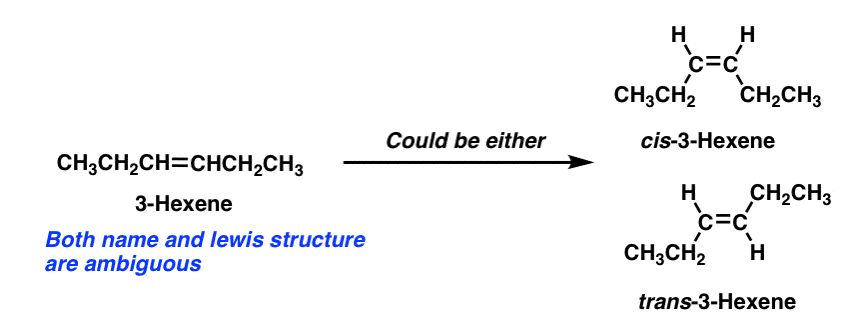
nota que 1-hexeno ainda está OK, uma vez que a 1-posição de 1-hexeno está ligada a dois grupos idênticos (hidrogénios) e, portanto, não são possíveis isómeros cis–trans.4. Cis-Trans-isomerismo para alcenos cíclicos
cis-e trans também pode ser aplicado a alcenos em anéis. Por exemplo, no papel é possível desenhar cis– e trans– ciclo – hexeno, uma vez que a ligação pi cumpre os requisitos para o cis – trans-isomerismo. Na realidade, o trans-ciclo-hexeno é impossivelmente tenso. Tenta beijar-te no cóccix., Isso dar– lhe-á uma ideia da tensão envolvida na tentativa de acomodar uma ligação trans-dupla num anel de seis membros .
Por esta razão, para os tamanhos de anel 7 e abaixo, é seguro ignorar a escrita “cis”: a configuração é assumida.
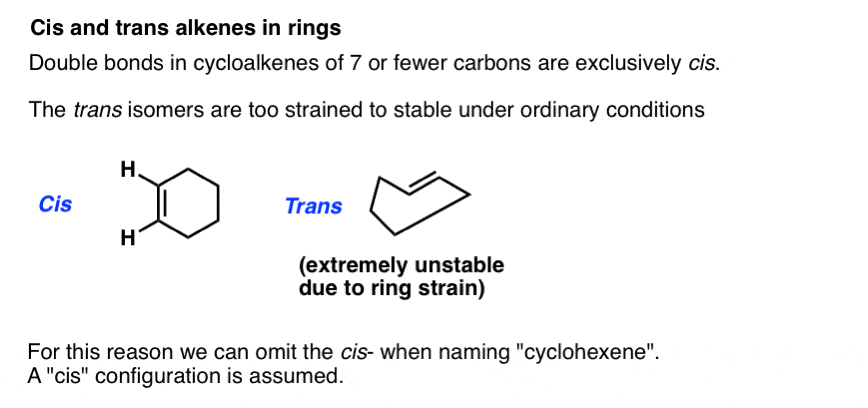
em anéis de 8 ou mais, precisamos de colocar um cis– ou trans – no nome, porque o trans– isómero torna-se viável. (Imagine tentar beijar-se no cóccix se você tivesse o pescoço de uma girafa: de repente não é impossível!,)
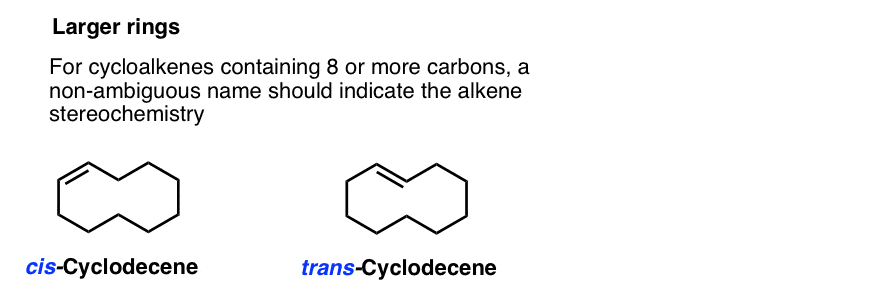
Uma Solução Para Quando “Cis” e “Trans” Falha: A E/Z Sistema
vimos que o cis e trans falha em anéis quando os dois carbonos faltou um comum substituinte. Também falha para alcenos nestas circunstâncias.caso em questão: tentar aplicar cis e trans ao alqueno abaixo:
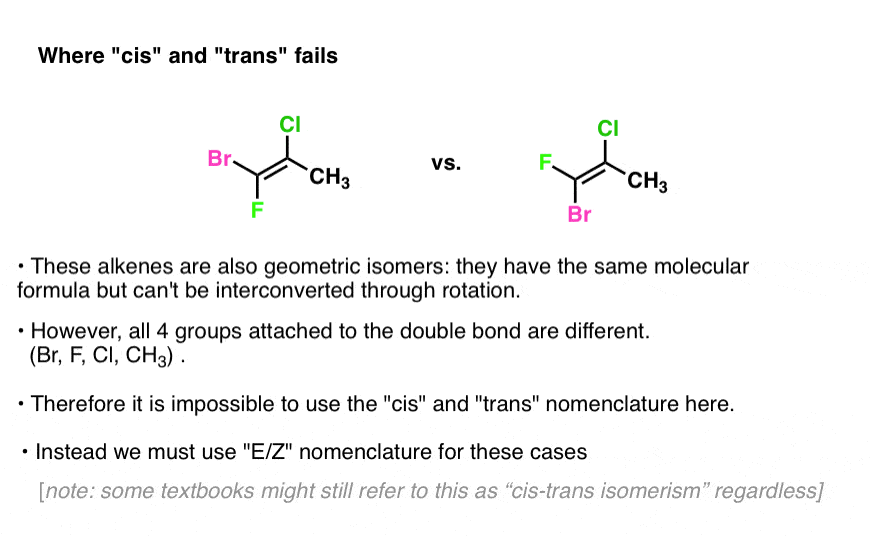
ver o problema?
na ausência de dois grupos idênticos, não temos ponto de referência!
à esquerda, o cloro é cis para Br e trans para F. Mas isso realmente justifica chamar o isômero “cis”? Como decidimos?,o que precisamos é de alguma forma de determinar prioridades nestas situações.
a notação E E Z para alcenos
felizmente, podemos aplicar o sistema de classificação desenvolvido por Cahn, Ingold, e Prelog para centros quirais (como tocado neste post anterior sobre (R)/(S) nomenclatura) para este propósito.
O Protocolo é o seguinte:
- Cada carbono na ligação pi Está ligado a dois substituintes. Para cada carbono, estes dois substituintes são classificados (1 ou 2) de acordo com os números atômicos do átomo diretamente ligado ao carbono. (como., Cl > F)
- Se ambos os substituintes classificados 1 estiverem do mesmo lado da ligação pi, A ligação recebe o descritor Z (abreviatura de zusammen alemão, que significa “juntos”).
- Se ambos os substituintes classificados no 1 estiverem do lado oposto da ligação pi, é-lhe atribuído o descritor E (abreviatura de entgegen alemão, que significa “oposto”).
assim Z assemelha-se a” cis “e e assemelha-se a” trans”. (Nota: eles não são necessariamente os mesmos e nem sempre correlacionam :Ver nota de rodapé para um exemplo de um alqueno cis que é E., O sistema E / Z é abrangente para todos os alcenos capazes de isomerismo geométrico, incluindo os exemplos cis/trans de alceno acima. Muitas vezes usamos cis/trans para conveniência, mas e/Z é o “oficial”, IUPAC aprovou a forma de nomear estereoisômeros de alceno].
uma maneira fácil de lembrar Z é dizer “Zee Zame Zide” em um sotaque alemão. A minha maneira de o fazer era fingir que o ” Z “significa ” zis”. O que funcionar para ti.,
Aqui está um exemplo prático:
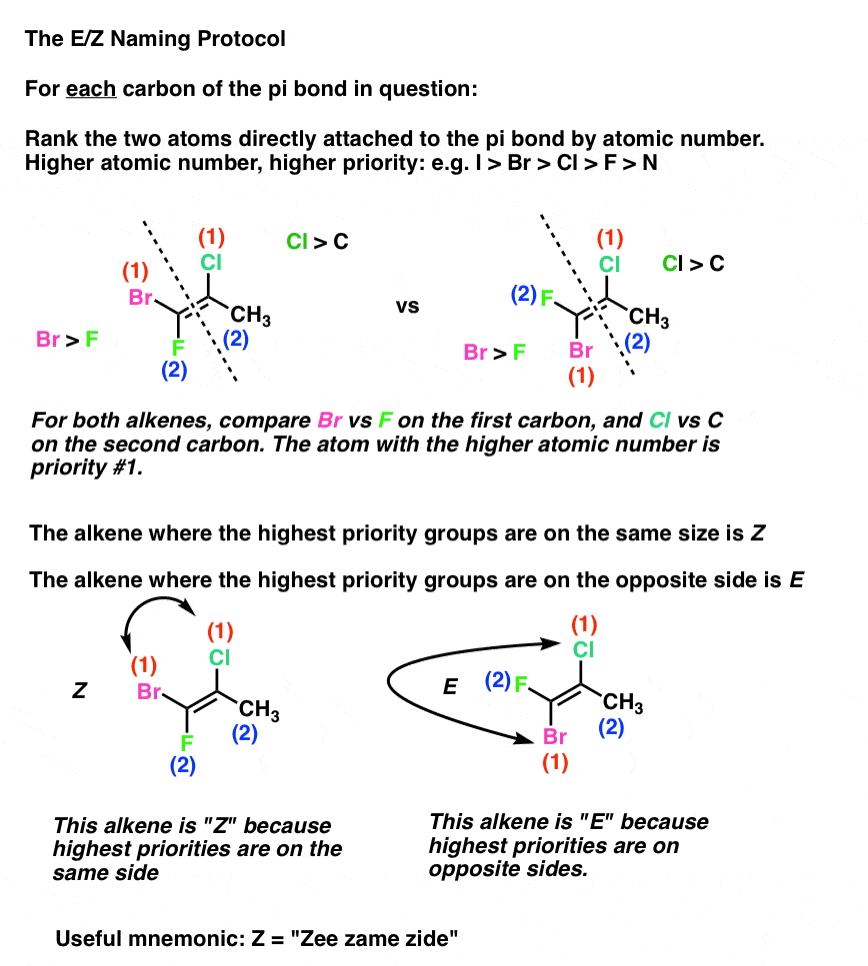
Como com centros quirais, classificação, de acordo com número atômico pode resultar em laços se nos restringimos apenas aos átomos diretamente ligados ao pi obrigações.
7. Breaking Ties: the Method of Dots
For instance, the alkene below presents us with a dilemma: one of the carbons of the alkene is attached to two carbon atoms. Então, como determinamos as prioridades neste caso? Como quebramos laços?
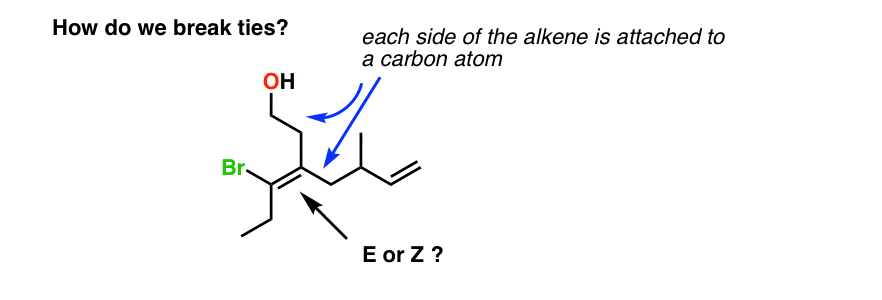
No caso de ligações, devemos aplicar o método dos pontos., Os pontos são substituições úteis e é por isso que gosto de usar este método.
- coloque um ponto em cada um dos dois átomos que está a comparar.
- listar os 3 átomos a que cada átomo está ligado, por ordem de número atómico.
- Compare as listas, assim como você compararia um conjunto de três cartas de jogar. Assim como uma mão de (8, 8, 7) batia (8, 7, 7), também batia (C, C, H) batia (C, H, H).se as listas forem idênticas, mova os pontos para o átomo de maior prioridade da lista.
- no primeiro ponto de diferença, atribuir (e ou Z).,
- Se não houver diferença … então os grupos são idênticos, e E / Z não se aplica.
Aqui está um exemplo prático do “método dos pontos”. 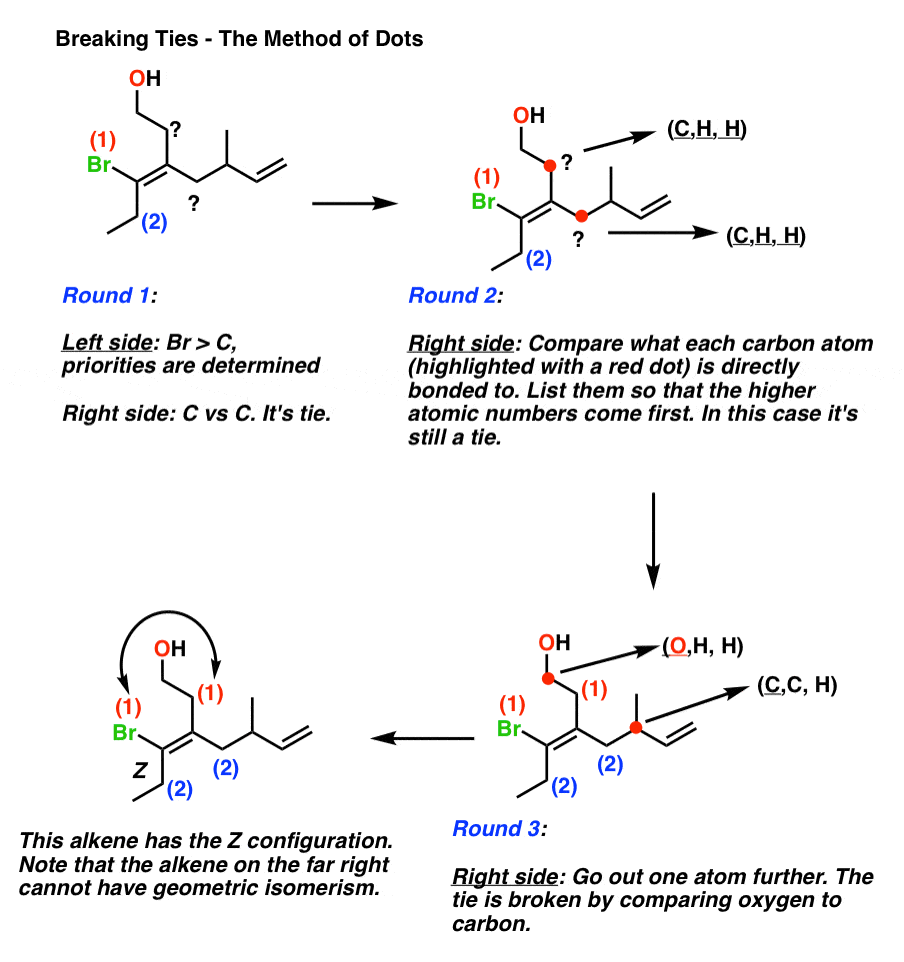
Aqui está um exemplo mais complexo com múltiplos alcenos. Neste caso, cada ligação pi é designada por um número com a sua própria configuração e ou Z.
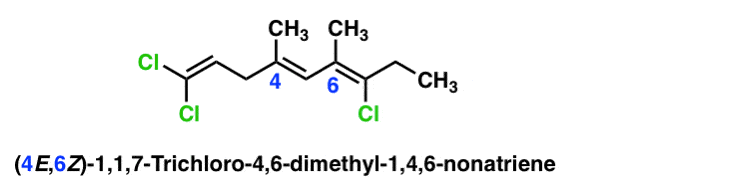
OK, esta foi longa. Mas espero que seja útil.
cuidado para um futuro post no qual vamos em mais detalhes sobre o “método dos pontos”.
8., Conclusão: a notação E E Z para alcenos
cis-trans – é OK para descrever estereoisómeros simples de alceno, mas só funciona em certos casos. Além disso, só dá configurações relativas. O sistema E / Z é abrangente e descreve a configuração absoluta da molécula.
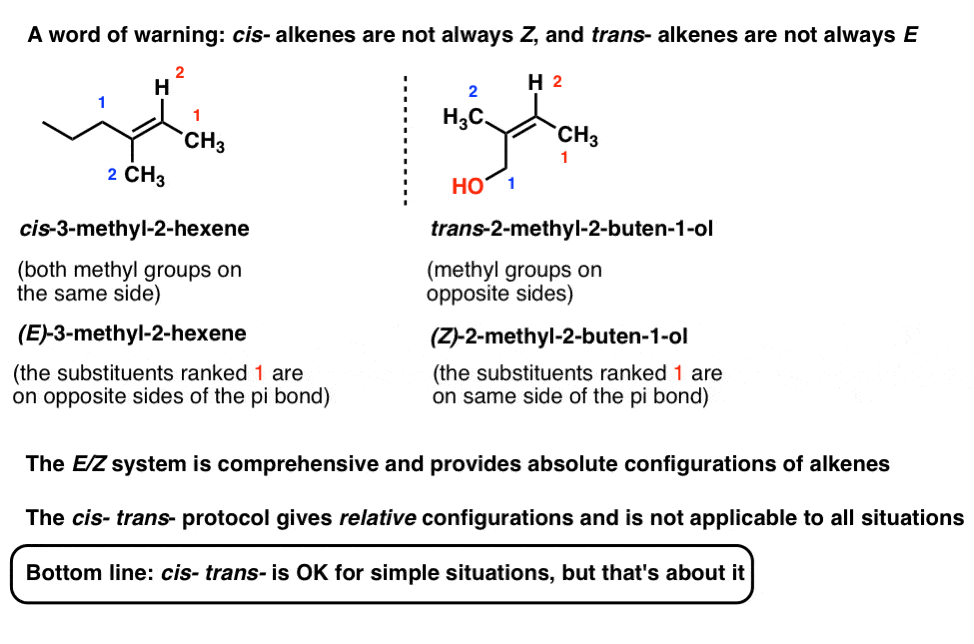
ver abaixo um exemplo de um E alceno que é ” cis “e um Z alceno que é”trans”.
apenas um lembrete: este post foi co-autor de Matt Pierce das soluções de Química Orgânica. Pergunte ao Matt sobre agendar uma sessão de explicações online aqui.,
notas
Nota 1: é possível ter um alceno que descreveríamos como ” cis ” e vice-versa.
E / Z é a nomenclatura preferida, mais abrangente, uma vez que descreve a configuração absoluta, enquanto cis – trans – apenas descreve a configuração relativa.
Nota 2: trans-ciclopropeno, trans-ciclobuteno e trans-ciclopenteno nunca foram sintetizados ou observados. o trans-ciclo-hexeno é uma curiosidade laboratorial, estável a poucos graus acima do zero absoluto. trans-ciclohepteno tem uma semi-vida extremamente curta à temperatura ambiente., trans-cyclooctene é uma molécula estável .pergunta a ti próprio!,v>
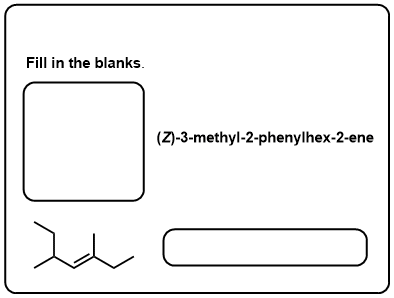 Clique para Virar
Clique para Virar 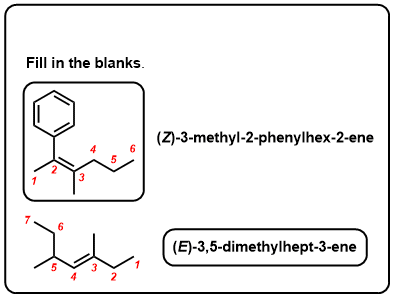
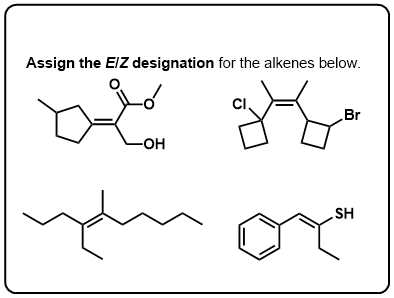 Clique para Virar
Clique para Virar 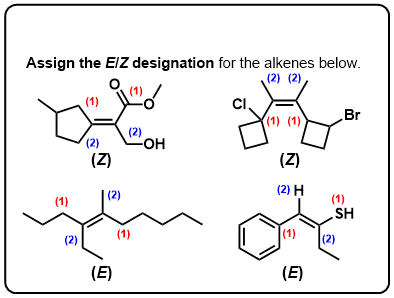
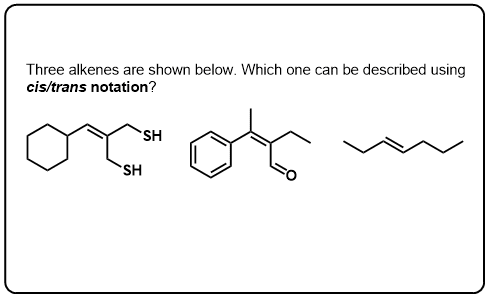 Clique para Virar
Clique para Virar 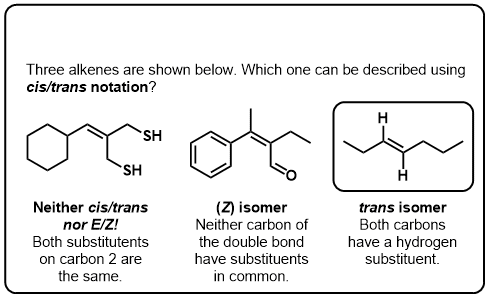
 Clique para Virar
Clique para Virar 