Vytvořené MakeTheBrainHappy.
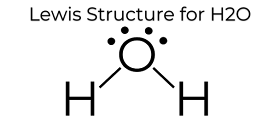
Lewisova Dot struktura H2O mu dává mnoho jedinečných vlastností hlavně díky dvěma osamělým párům na centrálním atomu kyslíku. To zvyšuje odpuzování elektronů a elektronů, a proto vytváří ohnutou strukturu na rozdíl od lineární struktury CO2. Tato“ ohnutá “ molekulární struktura mu dává mnoho jedinečných vlastností, jako je polární., Jedním z nejvíce fascinujících jevů je myšlenka „vodíkové vazby“, která dramaticky ovlivňuje vlastnosti vody.
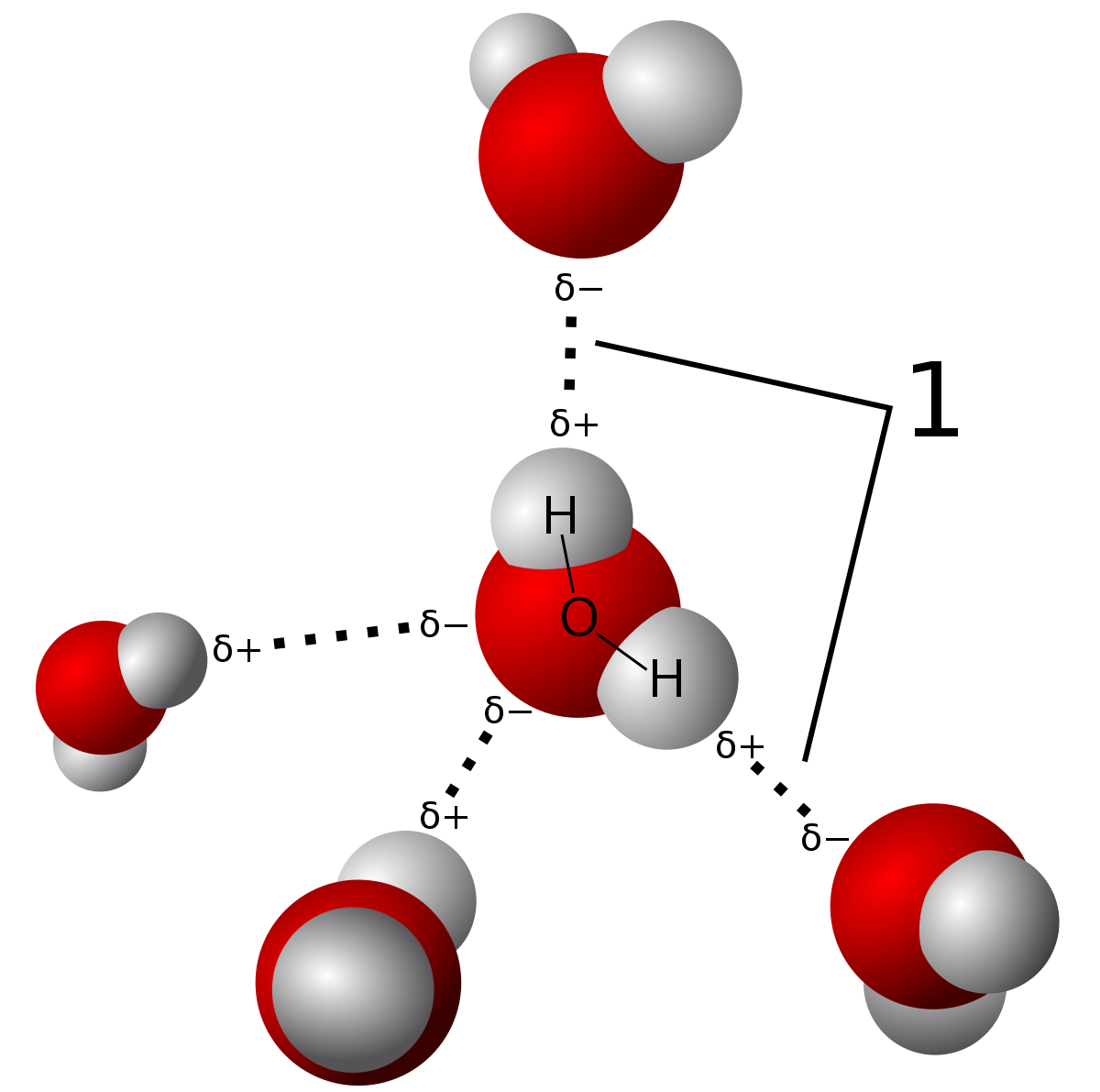
Vodíkové vazby je typ mezimolekulárních sil, kde rozdíl v elektronegativitě kyslíku, atom způsobuje částečnou permanentní dipól tvoří mezi atomy vodíku a kyslíku (viz čárkovaná linie). Vazby v samotné molekule vody jsou kovalentní vazby. Můžete se dozvědět o rozdílu v tomto příspěvku., Zdroj
Vzhledem k síle těchto vodíkových vazeb, voda má relativně vysokým bodem tání a bodu varu, i když nejsou tak vysoké jako síť kovalentní pevné látky. Ty jsou spojeny intramolekulárními silami, které zahrnují skutečné sdílení elektronů vs. částečné dipólové síly ve vodíkových vazbách. Existují pouze tři typy vazeb, které mohou vodíkové vazby. Jedná se o vazby N-H, O-H A F-H v důsledku velkých rozdílů elektronegativity mezi molekulami.,
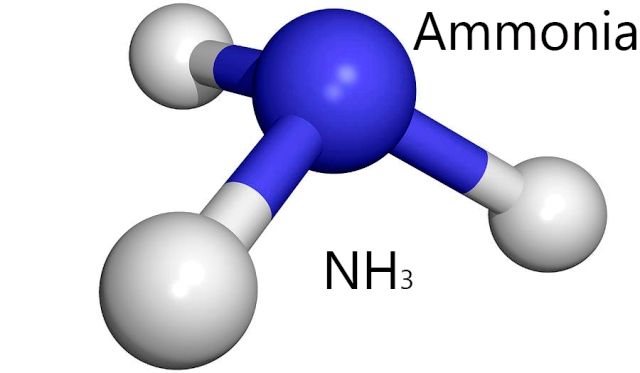
NH3 je další molekula, která vytváří podobné vodíkové vazby jako H2O. Zdroj
Jaké další vlastnosti má voda?
Voda je jedním z jediných prvků, které se nacházejí ve všech třech stavech (pevné, kapalné a plynné) přirozeně na zemi. Vodíkové spojení způsobuje krystalickou strukturu, která je méně hustá než kapalná voda. To je důvod, proč led plave v oceánech. Voda má také vysoké povrchové napětí a přilnavost., Soudržnost a přilnavost jsou nezbytné pro rostliny, které manipulují s těmito procesy, aby přesunuly vodu z kořenů do listů, aby podpořily růst rostliny. To vše je způsobeno jednoduchou strukturou H2O, představovanou výše uvedeným Lewisovým bodovým diagramem.

molekuly Vody ve všech třech skupenstvích. Zdroj